下列解释实验现象的离子反应方程式正确的是( )
| A、硫酸铵溶液显酸性:NH4++H2O?NH3?H2O+H+ |
| B、向AgCl悬浊液中加Na2S溶液,白色沉淀变成黑色:2Ag++S2-=Ag2S↓ |
| C、将足量CO2通入Na2SiO3溶液中,出现白色沉淀:SiO32-+CO2+H2O═H2SiO3↓+CO32- |
| D、向Na[Al(OH)4]溶液中加入NaHCO3溶液,出现白色沉淀:[Al(OH)4]++HCO3-═Al(OH)3↓+H2O+CO2 |
下列说法中,正确的是( )
| A、钢铁发生电化学腐蚀的正极反应式:Fe-2e-═Fe2+ |
| B、氢氧燃料电池的负极反应式:O2+2H2O+4e-═4OH- |
| C、电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-═Cl2↑ |
| D、粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e-═Cu2+ |
实验证明:若用电解熔融KCl制钾,发现钾熔于熔融KCl中难分离,且电解过程中容易发生爆炸事故等.因而工业不用电解熔融KCl制钾,而用金属钠与KCl共熔置换制钾:
Na(l)+KCl(l)?NaCl(l)+K(g)△H>0. 下面是四种物质的熔沸点:
根据平衡移动原理,可推知用Na与KCl反应制取金属钾的适宜温度是( )
Na(l)+KCl(l)?NaCl(l)+K(g)△H>0. 下面是四种物质的熔沸点:
| K | Na | KCl | NaCl | |
| 熔点/℃ | 63.6 | 97.8 | 770 | 801 |
| 沸点/℃ | 774 | 882.9 | 1500 | 1413 |
| A、低于770℃ |
| B、约850℃? |
| C、高于882.9℃ |
| D、1413~1500℃? |
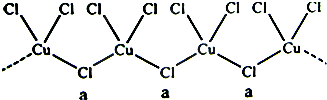
氯和钾与不同价态的铜可生成两种化合物,这两种化合物都可用于催化乙炔聚合,其阴离子均为无限长链结构(如图),a位置上Cl原子的杂化轨道类型为( )

| A、sp杂化 |
| B、sp2杂化 |
| C、sp3杂化 |
| D、dsp2杂化 |
甲醇(CH3OH)是一种洁净、可再生能源.生物质气(主要成分为CO、CO2、H2等),在含有Zn、Cu等元素的催化剂条件下能合成甲醇(CH3OH).下列说法不正确的是( )
| A、N2与CO互为等电子体 |
| B、CO2分子中碳原子的杂化类型是sp杂化,甲醇中碳原子的杂化类型是sp3杂化 |
| C、Zn在元素周期表中属于ds区,其晶体属于六方最密堆积,它的配位数是6 |
| D、Cu的外围电子排布式:3d104s1 |
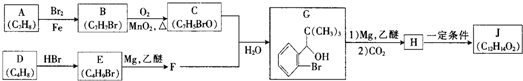
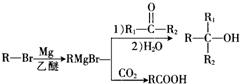
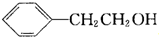 .
.