如图所示,a、b两电极材料分别为铁棒和铜棒,则下列说法中不正确的是( )


| A、该装置可以构成原电池,也可构成电解池 |
| B、a极可能发生反应:Cu2++2e-═Cu |
| C、b电极质量可能增加 |
| D、该过程可能有大量气体产生 |
室温下,pH相同体积相同的醋酸和盐酸两种溶液分别采取下列措施,有关叙述正确的是( )
| A、加水稀释2倍后,两溶液的pH均减小 |
| B、使温度都升高20℃后,两溶液的pH均不变 |
| C、加适量的醋酸钠晶体后,两溶液的pH均增大 |
| D、加足量的锌充分反应后,醋酸产生的氢气比盐酸少 |
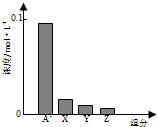 常温下,0.2mol?L-1的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法不正确的是( )
常温下,0.2mol?L-1的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法不正确的是( )| A、HA为弱酸 |
| B、该混合液pH>7 |
| C、图中X表示HA,Y表示OH-,Z表示H+ |
| D、该混合溶液中:c(A-)+c(Y)=c(Na+) |
已知25℃时有关弱酸的电离平衡常数如下表:下列推断正确的是( )
| 弱酸化学式 | HF | CH3COOH | HClO | H2CO3 |
| 电离常数 | 6.8×10-4 | 1.7×10-5 | 4.7×10-8 | K1=4.3×10-7 K2=5.6×10-11 |
| A、弱酸的酸性强弱:HF<HClO |
| B、同物质的量浓度NaClO与NaHCO3溶液,前者的pH较大 |
| C、将碳酸钠粉末加入到0.1mol?L_1 HClO溶液中,不发生反应 |
| D、中和等体积、等pH的HF和CH3COOH溶液,消耗等量的NaOH |
已知下面三个数据:7.2×10-4、4.6×10-4、4.9×10-10 分别是下列有关的三种酸的电离常数,若已知下列反应可以发生:NaCN+HNO2=HCN+NaNO2 NaCN+HF=HCN+NaF NaNO2+HF=HNO2+NaF由此可判断下列叙述不正确的是( )
| A、K(HF)=7.2×10-4 |
| B、K(HNO2)=4.9×10-10 |
| C、根据两个反应即可得出结论 |
| D、Ka(HCN)<Ka(HNO2 ) |


 (1)稀释0.1mol?L-1氨水时,随着水量的增加而减小的是
(1)稀释0.1mol?L-1氨水时,随着水量的增加而减小的是