 N2(g)+3H2(g)≒2NH3(g)△H=-92.2KJ/mol.在2L恒容密闭容器中各物质的浓度随时间变化的曲线如图所示.下列说法错误的是( )
N2(g)+3H2(g)≒2NH3(g)△H=-92.2KJ/mol.在2L恒容密闭容器中各物质的浓度随时间变化的曲线如图所示.下列说法错误的是( )| A、若时段I中投入物质的浓度为原来的2 倍,则反应物的转化率增大,平衡常数不变 |
| B、第25min改变的条件是将NH3从反应体系中分离出去 |
| C、若第60min时反应又达到了平衡,则时段Ⅲ改变的条件是降低温度 |
| D、前25min内反应放出的热量为46.lkJ |
足量的盐酸与下列物质反应,所得气体在同温同压下体积相同的一组物质是( )
| A、等物质的量的Na2CO3和NaHCO3 |
| B、等物质的量的Mg和CaCO3 |
| C、等质量的Na和Mg |
| D、等质量的Na2CO3和NaHCO3 |
相同温度下,在甲、乙、丙、丁四个烧杯中分别盛有等体积、等物质的量浓度的NaOH不饱和溶液,分别加入Na、Na2O、Na2O2、NaOH并恢复至原温度,使恰好都形成NaOH饱和溶液,则甲、乙、丙、丁四烧杯中加入的固体质量大小顺序是( )
| A、丁>丙>乙>甲 |
| B、丁>甲>乙>丙 |
| C、甲=丁>乙=丙 |
| D、丁<丙<乙<甲 |
图象可直观地描述化学反应的进程或结果,下列图象正确的是( )
A、 反应的正方向放热(t1时升温) |
B、 SO2气体通入氯气中 |
C、 NaOH溶液滴入Ca(HCO3)2溶液中 |
D、 将pH相同的NH4Cl溶液和稀盐酸稀释时pH的变化 |
 常温下,将1mL pH=2的一元酸HA溶液加水稀释至100mL,其pH与溶液体积(V)的关系如图所示,下列说法正确的是( )
常温下,将1mL pH=2的一元酸HA溶液加水稀释至100mL,其pH与溶液体积(V)的关系如图所示,下列说法正确的是( )| A、加热HA溶液时,溶液酸性增强 |
| B、1 mol?L-1 HA溶液与1 mol?L-1 NaOH溶液等体积混合,所得溶液中c(Na+)>c(A-),则2<a<4 |
| C、某浓度的NaA溶液的pH=d,则其中由水电离出的c(OH-)=1014-d mol?L-1 |
| D、HA溶液与NaOH溶液恰好完全反应时,c(Na+)>c(A-)>c(OH-)>c(H+) |
pH=2 的两弱酸HA、HB加水稀释后,溶液 pH随加水量的变化曲线如图所示.则下列叙述正确的是( )


| A、电离平衡常数HA<HB |
| B、等体积的HA 和HB与等浓度的NaOH反应,HA消耗的NaOH多 |
| C、等体积的HA和HB 与Zn反应,HB反应速率大 |
| D、等浓度的NaA、NaB,碱性NaA>NaB |

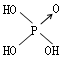
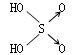
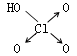
 据报道,在一定条件下,N2在掺有少量氧化铁的二氧化钛催化剂表面能与水发生反应,主要产物为NH3,相应的反应方程式为:2N2(g)+6H2O (g)?4NH3(g)+3O2(g)△H=Q kJ/mol
据报道,在一定条件下,N2在掺有少量氧化铁的二氧化钛催化剂表面能与水发生反应,主要产物为NH3,相应的反应方程式为:2N2(g)+6H2O (g)?4NH3(g)+3O2(g)△H=Q kJ/mol