设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A、1mol[Cu(NH3)2]2+中含有σ键的数目为12NA |
| B、0.1mol铁粉与足量水蒸气反应生成的H2分子数目为0.1NA |
| C、分子数目为0.1NA的N2和NH3混合气体,原子间含有的公共电子数目为0.3NA |
| D、用惰性电极电解CuSO4溶液一段时间后,若加入0.05mol的Cu2(OH)2CO3固体恰好能使溶液恢复到原来的浓度,则该电解过程中转移电子的数目为0.2NA |
以溴乙烷为主要原料制取乙二醇时,需要经过的反应为( )
| A、加成-消去-取代 |
| B、取代-消去-加成 |
| C、取代-加成-消去 |
| D、消去-加成-取代 |
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
A、常温下,78g的苯含有3NA个 双键 双键 |
| B、1L 0.1 mol?L-1的NH4Cl溶液中有0.1NA个NH4+ |
| C、标准状况下,22.4 L SO2与CO2混合物含有2NA个O原子 |
| D、常温下,5.6 g铁块投入足量浓硝酸中失去0.3NA个电子 |
下列说法中,错误的是( )
| A、含有离子键的化合物一定是离子化合物 |
| B、含有共价键的化合物一定是共价化合物 |
| C、共价化合物中一定含有极性共价键,肯定不含离子键 |
| D、离子化合物一定含有离子键,可能含有共价键. |
设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A、常温常压下,8 g甲烷中含C-H键的数目为4NA |
| B、25℃时,1L pH=13的Ba(OH)2溶液中含有的OH-数为0.2NA |
| C、1 mol冰醋酸和1 mol乙醇经催化加热反应生成H2O分子数为NA |
| D、标准状况下,2.24LCl2与过量稀NaOH溶液反应,转移的电子总数为0.1NA |
下列各装置能构成原电池的是( )
A、 |
B、 |
C、 |
D、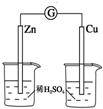 |
某药物中间体X,其结构如图所示.下列说法正确的是( )


| A、X分子中含有手性碳原子 |
| B、X可发生氧化、消去、取代等反应 |
| C、X既能与盐酸反应,又能与NaOH溶液反应 |
| D、1mol X与H2反应,最多消耗4mol H2 |
甲醇(CH3OH)是一种有毒物质,检测甲醇含量的测试仪工作原理示意图如下.下列说法正确的是( )

| A、该装置为电能转化为化学能的装置 |
| B、a电极发生的电极反应为CH3OH-6e-+H2O═CO2↑+6H+ |
| C、当电路中有1 mol e-转移时,正极区n(H+)增加1 mol |
| D、将酸性电解质溶液改为碱性电解质溶液该测试仪不可能产生电流 |
某有机物的结构为如图所示,该有机物不可能具有的性质是( )


| A、能使酸性KMnO4溶液褪色 |
| B、常温条件下为气体 |
| C、能跟NaOH溶液反应 |
| D、能发生酯化反应 |
