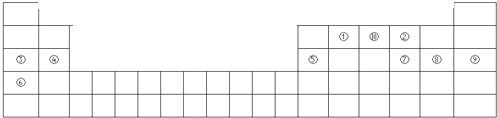
短周期元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为13,X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍或者是Y原子最外层电子数的3倍,下列说法正确的是( )
| A、X的氢化物溶于水生成弱酸 |
| B、Z的氢化物的水溶液在空气中存放不易变质 |
| C、Y与X可生成Y3X2型化合物 |
| D、Z的单质在氧气中燃烧可以生成两种酸性氧化物 |
在一定条件下,HA溶液存在电离平衡:HA?H++A--Q.下列说法正确的是( )
| A、稀释溶液,HA电离平衡常数增大 |
| B、升高温度,HA电离程度增大 |
| C、加入NaA固体,平衡朝正反应方向移动 |
| D、加入NaOH固体,溶液pH减小 |
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的一种反应原理如下:CH3OH(g)+H2O(g)═CO2(g)+3H2(g)△H=+49.0kJ?mol-1下列说法正确的是( )
| A、1 L CH3OH蒸气与1 L水蒸气反应生成1 L CO2气体与3 L氢气吸收热量49.0 kJ |
| B、1个CH3OH分子与1个水分子反应生成1个CO2分子与3个H2分子吸收49.0 kJ 热量 |
| C、相同条件下1 mol CH3OH(g)与1 mol H2O(g)的能量总和小于1 mol CO2(g)与3 mol H2(g)的能量总和 |
| D、1 mol CH3OH蒸气与1 mol液态水反应生成1 mol CO2气体与3 mol氢气吸收的热量小于49.0 kJ |
 某温度下,相同pH的盐酸和醋酸溶液分别加水稀释,pH随溶液体积变化的曲线如图所示.下列判断正确的是( )
某温度下,相同pH的盐酸和醋酸溶液分别加水稀释,pH随溶液体积变化的曲线如图所示.下列判断正确的是( )| A、相同体积时,c点溶液中和碱的能力大于a点 |
| B、b点溶液的导电性比c点溶液的导电性强 |
| C、b点酸的浓度大于a点酸的浓度 |
| D、Ⅱ为盐酸稀释时的pH变化曲线 |
高氯酸、硫酸、硝酸和盐酸都是强酸,其酸性在水溶液中差别不大.以下是某温度下这四种酸在冰醋酸中的电离常数从表格中判断以下说法中不正确的是( )
| 酸 | HClO4 | H2SO4 | HCl | HNO3 |
| Ka | 1.6×10-5 | 6.3×10-9 | 1.6×10-9 | 4.2×10-10 |
| A、在冰醋酸中这四种酸都没有完全电离 |
| B、在冰醋酸中高氯酸是这四种酸中最强的酸 |
| C、在冰醋酸中硫酸的电离方程式为H2SO4=2H++SO42- |
| D、酸的强弱与其本身的结构和溶剂的性质有关 |
 标出原电池的电极材料和电解质溶液,并写出负极的电极反应为
标出原电池的电极材料和电解质溶液,并写出负极的电极反应为