用铁片与稀硫酸反应制取氢气时,下列措施不能使氢气生成速率加大的是( )
| A、热的稀硫酸 |
| B、不用稀硫酸,改用98%浓硫酸 |
| C、滴加少量AgNO3溶液 |
| D、不用铁片,改用铁粉 |
下列说法正确的是( )
| A、在pH=10的氨水中加水稀释时,溶液中所有离子的浓度都减小 |
| B、中和pH相同的盐酸和醋酸,醋酸消耗同浓度的氢氧化钠体积多 |
| C、将pH=9的NaOH、CH3COONa溶液等体积混合:c(Na+)=c(CH3COO-)+c(OH-)-c(H+) |
| D、0.1mol?L-1HA中加入少量NaA固体,HA的电离平衡逆向移动,HA的电离常数减小 |
今有室温下四种溶液,有关叙述不正确的是( )
| ① | ② | ③ | ④ | |
| 浓度c/mol/L | 0.1 | 0.1 | 0.1 | 0.1 |
| 溶液 | 氨水 | CH3COONa溶液 | 醋酸 | 盐酸 |
A、 在20 mL ①溶液中逐滴加入③溶液,溶液导电能力变化如图 |
| B、②、③两溶液等体积混合,离子浓度:2c(Na+)=c(CH3COO-)+c(CH3COOH) |
| C、①、④两溶液等体积混合,离子浓度:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
D、 用④滴定①,滴定曲线如图,可用酚酞作指示剂 |
下列有关热化学方程式的叙述正确的是( )
| A、已知C(石墨,s)→C(金刚石,s);△H>0,则金刚石比石墨稳定 | ||
B、已知C(s)+O2(g)→CO2(g);△H1和C(s)+
| ||
| C、在101KPa时,2 H2 (g)+O2 (g)=2 H2O(l);△H=-571.6kJ?mol-1,则2mol液态水分解成2mol氢气和1mol氧气吸收571.6KJ的热量 | ||
| D、含20.0gNaOH的稀溶液与稀盐酸完全中和时放出28.7kJ的热量,则该反应的热化学方程式为:NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l);△H=+57.4 kJ?mol-1 |
下列各反应中电子转移方向和数目表示正确的是( )
A、 |
B、 |
C、 |
D、 |
获2009年中国科技创业大赛最高奖的“超薄型软电池”的总反应为:Zn+2MnO2+2H2O═Zn(OH)2+2MnO(OH).下列说法正确的是( )
| A、该电池中Zn作负极,发生还原反应 |
| B、该电池工作时电流由Zn经导线流向MnO2 |
| C、该电池正极反应式为:2MnO2+2e-+2H2O═2MnO(OH)+2OH- |
| D、该电池工作时,若电路中转移2NA个电子(NA为阿伏加德罗常数),则负极质量减少约65g |
下列各组的电极材料和电解液,不能组成原电池的是( )
| A、铁棒 铁棒,稀硫酸 |
| B、铜片、石墨棒,硝酸银溶液 |
| C、锌片、铜片,稀盐酸 |
| D、铜片、银片,FeCl3溶液 |
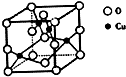 超细铜粉主要应用于导电材料、催化剂等领域中.超细铜粉的某制备方法如下:
超细铜粉主要应用于导电材料、催化剂等领域中.超细铜粉的某制备方法如下: