已知1-18号元素的离子aW3+、bX+、CY2-、dZ-都具有相同的电子层结构,则下列叙述或表示方法正确的是( )
| A、四种元素位于同一周期 |
| B、氢化物的稳定性H2Y>HZ |
| C、离子的氧化性aW3+>bX+ |
| D、a+3<c-2 |
据人民网报道,有一集团拟在太空建立巨大的激光装置,把太阳光变成激光用于分解海水制氢气,其反应式可表示为:2H2O
2H2↑+O2↑.有下列几种说法:
①水的分解反应是放热反应;
②氢气是一级能源;
③使用氢气作燃料有助于控制温室效应;
④该过程将光能转化为化学能,
以上叙述中正确的是( )
| ||
| 激光 |
①水的分解反应是放热反应;
②氢气是一级能源;
③使用氢气作燃料有助于控制温室效应;
④该过程将光能转化为化学能,
以上叙述中正确的是( )
| A、①② | B、②③ |
| C、③④ | D、①②③④ |
以下自发反应能用△H判据来解释的是( )
| A、硝酸铵自发地溶于水 |
| B、2N2O5(g)=4NO2 (g)+O2(g)△H=+156.7kJ/mol |
| C、(NH4)2CO3(s)=NH4HCO3(s)+NH3(g)△H=+74.9 kJ/mol |
| D、2H2(g)+O2(g)=2H2O(l)△H=-285.8kJ/mol |
能量越低,物质越稳定.反应:石墨→金刚石是吸热反应,由此可知( )
| A、石墨比金刚石更稳定 |
| B、石墨和金刚石可以相互转化 |
| C、金刚石比石墨更稳定 |
| D、石墨和金刚石不能互相转化 |
已知化学反应A2(g)+B2(g)═2AB(g)的能量变化如图所示,下列叙述中正确的是( )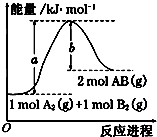

| A、该反应热△H=-(a-b) kJ?mol-1 |
| B、每生成2mol AB(g)吸收b kJ |
| C、该反应中反应物的总能量高于生成物的总能量 |
| D、该反应中反应物的总键能大于生成物的总键能 |
下列排序不正确的是( )
| A、熔点:CF4<CCl4 |
| B、熔点:K>Na |
| C、硬度:金刚石>碳化硅 |
| D、晶格能:NaF>NaCl |
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)═CO2(g)+3H2(g);△H=+49.0kJ?mol-1
②CH3OH(g)+
O2(g)═CO2(g)+2H2(g);△H=-192.9kJ?mol-1
下列说法正确的是( )
①CH3OH(g)+H2O(g)═CO2(g)+3H2(g);△H=+49.0kJ?mol-1
②CH3OH(g)+
| 1 |
| 2 |
下列说法正确的是( )
| A、若用甲醇(CH3OH)为原料设计成燃料电池,则通入甲醇的电极为负极 | ||
B、 反应①中的能量变化如图所示 | ||
| C、CH3OH转变成H2的过程一定要吸收能量 | ||
D、根据②推知反应:CH3OH(l)+
|
已知反应:CO(g)?C(s)+
O2(g)的△H为正值,△S为负值.设△H和△S不随温度而变化,下列说法中正确的是( )
| 1 |
| 2 |
| A、低温下是自发变化 |
| B、高温下是自发变化 |
| C、低温下是非自发变化,高温下是自发变化 |
| D、任何温度下都是非自发变化 |
在下列反应中,生成物的能量总和高于反应物的能量总和的是( )
| A、Zn(s)+CuSO4(aq)=ZnSO4(aq)+Cu(s)放热反应 |
| B、2CO(g)+O2(g)=2CO2(g)放热反应 |
| C、CaCO3(s)=CaO(s)+CO2(g)吸热反应 |
| D、H+(aq)+OH-(aq)=H2O(l)放热反应 |