如图所示的装置中铁棒上析出铜,而铁的质量不变,符合要求的原电池是( )


| A、铁棒作负极,铜棒作正极,电解质溶液是CuSO4溶液 |
| B、镁棒作负极,铁棒作正极,电解质溶液是CuSO4溶液 |
| C、镁棒作负极,铁棒作正极,电解质溶液是FeCl3溶液 |
| D、铁棒作负极,铜棒作正极,电解质溶液是H2SO4溶液 |
下列关于原电池的叙述中正确的是( )
| A、在锌、铜、CuSO4溶液组成的原电池中,负极质量减轻,正极质量增加 |
| B、在铁、铝、稀硫酸组成的原电池中,电子由铁片通过导线流向铝片 |
| C、在锌、铜、稀硫酸组成的原电池中,当电池工作时,硫酸根离子向正极移动 |
| D、在镁、铝、稀NaOH溶液组成的原电池中,镁是负极,铝是正极 |
下列装置能形成原电池且灵敏电流计发生偏转的是( )
A、 氯化铁溶液 |
B、 稀硫酸 |
C、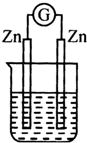 硫酸铜溶液 |
D、 乙醇 |
可逆反应2SO2+O2?2SO3,若用2mol SO2和1mol18O2在一定条件下,经足够长的时间反应,下列情况可能出现的是( )
| A、18O原子完全存在于三氧化硫中 |
| B、18O原子存在于氧气、二氧化硫、三氧化硫中 |
| C、生成2 mol三氧化硫 |
| D、二氧化硫、三氧化硫均为1.5mol |
电子表所用纽扣电池的两极材料为锌和氧化银,电解质为KOH溶液,其电极反应如下:锌极Zn+2OH--2e-═Zn(OH)2 氧化银Ag2O+H2O+2e-═2Ag+2OH-,下列说法正确的是( )
| A、锌为正极,被氧化 |
| B、氧化银为正极,被氧化 |
| C、电子从锌流向氧化银 |
| D、锌为负极,被还原 |
一定条件下,将A、B、C三种物质各1mol通入一个密闭容器中发生反应:2A+B?2C,达到化学反应限度时,B的物质的量可能是( )
| A、1.5mol | B、1mol |
| C、0.5mol | D、0 |
某溶液中含有较大浓度的H+、Fe2+、SO42-时,下列物质可以在其中大量存在的是( )
| A、CuCl2 |
| B、Cl2 |
| C、NaNO3 |
| D、NH3 |
已知25℃时,CaSO4在水中沉淀溶解平衡曲线如下图所示,向100mL该条件下的CaSO4饱和溶液中,加入400mL 0.01mol/L的Na2SO4溶液,针对此过程的下列叙述正确的是( )

| A、溶液中析出CaSO4固体沉淀,最终溶液中c(SO42-)较原来大 |
| B、溶液中无沉淀析出,溶液中c(Ca2+)、c(SO42-)都变小 |
| C、溶液中析出CaSO4固体沉淀,溶液中c(Ca2+)、c(SO42-)都变小 |
| D、溶液中无沉淀析出,但最终溶液中c(SO42-)较原来大 |
 王亮在超市看到一种电池外壳的纸层包装印有如图的文字,请根据要求回答
王亮在超市看到一种电池外壳的纸层包装印有如图的文字,请根据要求回答 若将反应2Fe3++Cu═Cu2++2Fe2+设计成原电池,请画出原电池的装置图,标出正、负极,并写出电极反应式.
若将反应2Fe3++Cu═Cu2++2Fe2+设计成原电池,请画出原电池的装置图,标出正、负极,并写出电极反应式.