下列表述正确的是( )
| A、100℃时,0.1 mol?L-1 HCl和NaOH溶液的pH分别为1和13 |
| B、将pH=4的醋酸溶液加水稀释后,溶液中所有离子的浓度均降低 |
| C、等体积、等pH的HCl和CH3 COOH溶液分别与NaOH溶液反应,CH3 COOH消耗NaOH的物质的量多 |
| D、在滴有酚酞溶液的氨水中,加入NH4Cl(溶液显酸性)至溶液无色,此时溶液一定显中性 |
25℃,水的电离达到平衡:H2O?H++OH-,下列叙述正确的是( )
| A、向水中加入冰醋酸,平衡逆向移动,c(H+)降低 |
| B、向水中加入少量固体碳酸氢钠,c(H+)增大,Kw不变 |
| C、向水中加入少量固体CH3COONa,平衡正向移动,c(H+)降低 |
| D、将水加热,Kw增大,pH不变 |
关于如图所示装置的叙述,错误的是( )


| A、锌是负极,其质量逐渐减小 |
| B、氢离子在铜片表面被还原,产生气泡 |
| C、电流从锌片经导线流向铜片 |
| D、电子从锌片经导线流向铜片 |
已知:Ksp(Fe(OH)3)=4.0×10-38,Ksp(Mg(OH)2)=1.8×10-11要除去MgCl2酸性溶液里少量的FeCl3,不宜选用的试剂是( )
| A、MgO |
| B、MgCO3 |
| C、NaOH |
| D、Mg(OH)2 |
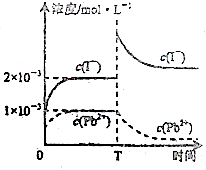 常温下,取一定量的PbI2固体配成饱和溶液,T时刻改变某一条件,离子浓度变化如图所示,下列有关说法正确的是( )
常温下,取一定量的PbI2固体配成饱和溶液,T时刻改变某一条件,离子浓度变化如图所示,下列有关说法正确的是( )| A、常温下,PbI2的Ksp为2×10-6 |
| B、温度不变,向PbI2饱和溶液中加入少量硝酸铅浓溶液,PbI2的溶解度不变,Pb2+浓度不变 |
| C、常温下Ksp[PbS]=8×10-28,向PbI2的悬浊液中加入Na2S溶液,PbI2(s)+S2-(aq)?PbS(s)+2I-(aq)反应的化学平衡常数为5×1018 |
| D、T时刻改变的条件是由于升高温度,PbI2的Ksp增大 |
有人设计出利用CH4和O2的反应,用铂电极在KOH溶液中构成原电池.电池的总反应为:CH4+2O2+2KOH=K2CO3+3H2O则下列说法正确的是( )
①通入甲烷的电极为电池的正极,
②通入氧气的电极为正极
③每有1molCH4被氧化,转移8mol电子
④电池放电后,溶液PH不断升高.
①通入甲烷的电极为电池的正极,
②通入氧气的电极为正极
③每有1molCH4被氧化,转移8mol电子
④电池放电后,溶液PH不断升高.
| A、①② | B、②③ | C、①④ | D、③④ |
如图所示的8个装置中能将化学能转化为电能的是( )


| A、①④ | B、③④⑤ |
| C、④⑧ | D、②④⑥⑦ |
CaCO3在下列液体中溶解度最大的是( )
| A、纯水中 |
| B、0.1 mol?L-1的Na2CO3溶液中 |
| C、0.1 mol?L-1的CaCl2溶液中 |
| D、0.1 mol?L-1的CH3COOH溶液中 |
