下列各组在溶液中的反应,不管反应物的量是多少,都能用同一离子方程式表示的是( )
| A、NaOH与CO2 |
| B、Ba(OH)2与H2SO4 |
| C、HC1与Na2CO3 |
| D、NaHCO3与Ca(OH)2 |
下列指定反应的离子方程式正确的是( )
| A、向Na2SiO3溶液中通入过量CO2:SiO32-+CO2+H2O═H2SiO3↓+CO32- |
| B、酸性介质中KMnO4氧化H2O2:2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O |
| C、等物质的量的MgCl2、Ba(OH)2 和 HC1 溶液混合:Mg2++2OH-═Mg(OH)2↓ |
| D、用CH3COOH溶解CaCO3:CaCO3+2H+═Ca2++H2O+CO2↑ |
下列离子方程式中不正确的是( )
| A、氢氧化钡溶液与硫酸混合:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O |
| B、饱和碳酸钠溶液通入二氧化碳后,溶液浑浊:2Na++CO32-+CO2+H2O═2NaHCO3↓ |
| C、氯化铝溶液与过量的氨水反应:Al 3++4NH3?H2O═AlO2-+4NH4++2H2O |
| D、氯气通入冷的氢氧化钠溶液中:Cl2+2OH-═Cl-+ClO-+H2O |
设NA为阿伏加德罗常数的数值.下列说法正确的是( )
| A、1mol甲苯含有6NA个C-H键 |
| B、18gH2O含有10NA个质子 |
| C、标准状况下,22.4L乙醇的分子数为NA |
| D、电解精炼铜过程中,电路中每通过NA个电子,阳极溶解铜32g |
设NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A、常温常压下,11.2 LCO2所含的原子数为1.5NA | ||
| B、常温常压下,48 g O3含有的氧原子数为3NA | ||
| C、标准状况下,22.4 L SO3中所含原子数为4NA | ||
D、标准状况下,1 L水所含分子数为
|
用NA表示阿伏加德罗常数的值,下列说法中不正确的是( )
| A、1 mol白磷(P4)晶体中,所含σ键的数目为4NA |
| B、1 mol Na2O2晶体中,所含离子总数为3NA |
| C、12 g金刚石中,所含C-C键的数目为2NA |
| D、1 mol SiO2晶体中,所含Si-O键的数目为4NA |
设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A、常温常压下,15g甲基(-CH3)中所含的中子数为6NA |
| B、一定条件下Fe粉与足量的浓硫酸反应,转移电子数为3NA |
| C、在1 L的碳酸钠溶液中,若c(CO32-)=1 mol?L-1,则溶液中Na+的个数为2NA |
| D、含4NA个离子的固体Na2O2溶于水配成1 L溶液,所得溶液中Na+的物质的量浓度为2 mol?L-1 |
下列说法正确的是(NA为阿伏加德罗常数的值)( )
| A、1mol甲基(-14C1H3)所含的中子数和电子数分别为8NA、9NA |
| B、0.1mol/L的Na2S溶液中,含Na+的数目为0.2NA |
| C、0.1molMnO2与40mL 10mol/L的浓盐酸充分反应,生成的氯气分子数为0.1NA |
| D、16.9 g过氧化钡(BaO2)加入足量H2O中转移电子数目为0.2NA |
下列化学用语表示正确的是( )
| A、乙烯的结构简式:CH2CH2 | ||
B、S2-的结构示意图: | ||
C、中子数为20的氯原子:
| ||
D、羟基的电子式: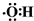 |