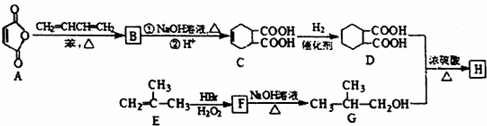
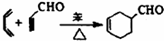
常温条件下,将0.01mol?L-1Na2CO3溶液与0.01mol?L-1KHCO3溶液等体积混合.若忽略混合后体积的变化,则下列判断正确的是( )
| A、两种溶液混合前,Na2CO3溶液中水电离出的c(H+)小于KHCO3溶液水电离出的c(H+) |
| B、混合后溶液中存在关系:c(CO32-)+c(HCO3-)+c(H2CO3)=0.02 mol?L-1 |
| C、混合后溶液中存在关系:c(K+)+c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-) |
| D、混合后溶液中存在关系:c(K+)+c(H2CO3)+c(H+)=c(CO32-)+c(OH-) |
在下列各用途中,利用了物质的氧化性的是( )
| A、用食盐腌制食物 |
| B、用漂粉精消毒游泳池中的水 |
| C、用汽油洗涤衣物上的油污 |
| D、用盐酸除去铁钉表面的铁锈 |
下列说法正确的是( )
| A、甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应 |
| B、分子式为C4H7ClO2,可与NaHCO3产生CO2的有机物可能结构有3种 |
C、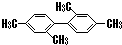 分子中至少有11个碳原子处于同一平面上 分子中至少有11个碳原子处于同一平面上 |
D、1mol有机物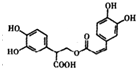 一定条件下能和7molNaOH反应. 一定条件下能和7molNaOH反应. |
以下是在实验室模拟“侯氏制碱法”生产流程的示意图:则下列叙述错误的是( )


| A、A气体是NH3,B气体是CO2 |
| B、把纯碱及第Ⅲ步所得晶体与某些固体酸性物质(如酒石酸)混合可制泡腾片 |
| C、第Ⅲ步操作用到的主要玻璃仪器是烧杯、漏斗、玻璃棒 |
| D、第Ⅳ步操作是将晶体溶于水后加热、蒸发、结晶 |
下列推断或表述正确的是( )
| A、25℃时,pH=4.7浓度均为0.1mol?L-1的CH2COOH、CH3COONa混合溶液中,c(CH3COO-)+c(OH-)<c(CH3COOH)+c(H+) |
| B、常温下,氨水与(NH4)2SO4溶液混合所得pH=7的溶液中,c(NH4+):c(SO42-)=2:1 |
| C、将体积相同,pH均为1的盐酸和醋酸分别加水稀释至pH=3,盐酸的体积变化大,证明醋酸是弱酸 |
| D、向2.0ml浓度均为0.1mol?L-1的KCl、KI混合液中滴加1-2滴0.01mol?L-1AgNO3溶液,振荡,沉淀呈黄色,说明AgCl的Ksp比AgI的Ksp小 |
水溶液中下列离子能大量共存的是( )
| A、K+、Fe3+、C6H5O-、HCO3- |
| B、H+、Cu2+、MnO4-、SO42- |
| C、Mg2+、Ag+、CO32-、NO3- |
| D、Na+、Al3+、BrO-、S2- |
下列各组离子可能大量共存的是( )
| A、不能使酚酞试液变红的无色溶液中:Na+、CO32-、K+、ClO- |
| B、能与金属铝反应放出氢气的溶液中:K+、NO3-、Cl-、NH4+ |
| C、常温下水电离出的c(H+)?c(OH-)=10-20的溶液中:Na+、Cl-、S2-、SO32- |
| D、无色透明溶液:K+、HCO3-、NO3-、SO42-、Fe3+ |
常温下,下列离子在指定条件下能大量共存的是( )
| A、c(I-)=0.1 mol/L的溶液中:Ca2+、NO3-、Fe3+、Cl- |
| B、SO2饱和溶液中:NH4+、K+、CO32-、ClO- |
| C、放入镁带有气体逸出的溶液中:Na+、K+、Cl-、SO42- |
| D、水电离出c(H+)=1×10-10mol/L溶液中:Cu2+、Na+、S2-、CH3COO- |