0 126979 126987 126993 126997 127003 127005 127009 127015 127017 127023 127029 127033 127035 127039 127045 127047 127053 127057 127059 127063 127065 127069 127071 127073 127074 127075 127077 127078 127079 127081 127083 127087 127089 127093 127095 127099 127105 127107 127113 127117 127119 127123 127129 127135 127137 127143 127147 127149 127155 127159 127165 127173 203614

 SO42—+Cr3++H2O(未配平),则每消耗0.4mol Cr2O72—转移__________mol e-。
SO42—+Cr3++H2O(未配平),则每消耗0.4mol Cr2O72—转移__________mol e-。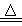 Na2S2O3(aq)
Na2S2O3(aq)
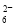 +2I-
+2I-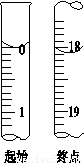
 2NO(g),是导致汽车尾气中含有NO的原因之一。
2NO(g),是导致汽车尾气中含有NO的原因之一。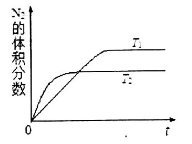

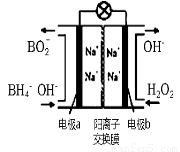
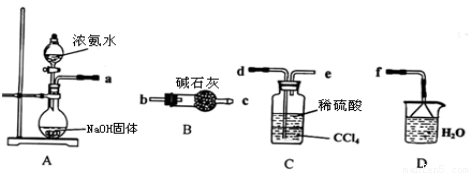
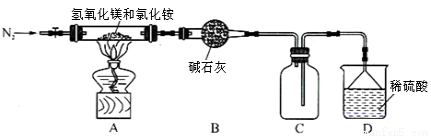
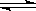 I3-(aq),该反应的平衡常数与温度的关系如下图,下列说法错误的是
I3-(aq),该反应的平衡常数与温度的关系如下图,下列说法错误的是