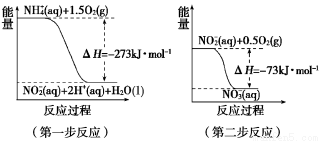
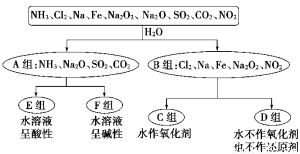
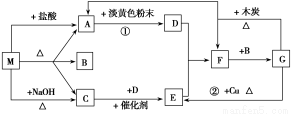
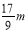(13分)现有铁、碳两种元素组成的合金,某实验小组为了研究该合金的性质并测定该合金中碳的质量分数,设计了如下实验方案和实验装置:
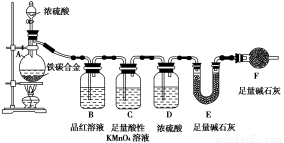
Ⅰ.探究该合金的某些性质:
(1)取a g合金粉末放入蒸馏烧瓶,并加入足量浓硫酸,A、B中均无明显现象,原因是_________________________________________________________________。
(2)点燃酒精灯一段时间后,A中剧烈反应,请写出A中反应的化学方程式:________________________________________。
(3)在盛有BaCl2溶液的C试管中,除了导管口有气泡外,无其他明显现象,若将其分成两份,分别滴加下列溶液,将产生沉淀的化学式填入下表相应的位置。
滴加的溶液 | 氯水 | 氨水 |
沉淀的化学式 |
Ⅱ.测定样品中碳的质量分数:
(4)装置F的作用是_______________________________________________________。
(5)反应结束后,若U形管E增重m g,则合金中碳的质量分数为________(用含m和a的式子表示)。若没有装置D,会使合金中碳的质量分数______ (填偏高、偏低、无影响)
(6)若将SO2气体通入含有n mol Na2S的溶液中,溶液中出现黄色浑浊,试分析该溶液最多能吸收SO2气体________mol(不考虑溶解的SO2)。

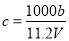 B.
B.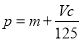
 <
<