(17分)FeBr2是一种黄绿色鳞片状的固体,某研究性学习小组为了探究它的还原性,进行了如下实验:
I:实验需要90mL 0.1mol/LFeBr2溶液
(1)配制FeBr2溶液除烧杯、玻璃棒、量筒、胶头滴管外还需的玻璃仪器是
(2)下列有关配制过程中说法正确的是 (填序号)。
a.用托盘天平称量质量为1.94g的FeBr2
b.将称量的FeBr2放入容量瓶中,加90mL蒸馏水溶解
c.洗涤溶解FeBr2的烧杯,并将洗涤液转移至容量瓶中
d.容量瓶贴签存放配好的FeBr2溶液
e.定容时,仰视容量瓶刻度线会使配制的FeBr2溶液浓度偏低
II:探究FeBr2的还原性
取10mL上述FeBr2溶液,向其中滴加少量新制的氯水,振荡后溶液呈黄色。某同学对产生黄色的原因提出了假设:
假设1:Br- 被Cl2氧化成Br2溶解在溶液中;
假设2:Fe2+ 被Cl2氧化成Fe3+。
请你完成下表,验证假设:
实验步骤、预期现象 | 结论 |
①向溶液中加入适量CCl4,振荡、静置后 现象:__________________________; | 假设1正确 |
②向溶液中加入 溶液 现象: 。 | 假设2正确 |
若假设1正确,从实验①中分离出Br2的实验主要操作名称是 ;
(2)实验证明:还原性Fe2+ > Br-
请用一个离子方程式来证明: ;
(3)若在50mL上述FeBr2溶液中通入5×10-3molCl2,则反应的离子方程式为: 。
(18分)
I:(10分)某无色废水中可能含有H+、NH、Fe3+、Al3+、Mg2+、Na+、NO、CO、SO中的几种,为分析其成分,分别取废水样品100 mL,进行了三组实验,其操作和有关图像如下所示:
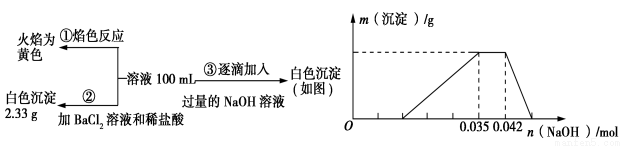
请回答下列问题:
(1)根据上述3组实验可以分析废水中一定不存在的离子有: 。
(2)写出实验③图像中沉淀溶解阶段发生的离子反应方程式: 。
(3)分析图像,在原溶液中c(NH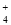 )与c(Al3+)的比值为 。NO
)与c(Al3+)的比值为 。NO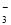 是否存在? 填(“存在”“不存在”或“不确定”)。
是否存在? 填(“存在”“不存在”或“不确定”)。
II:(8分)现有A、B、C、D、E五种可溶性强电解质,它们在水中可电离产生下列离子(各种离子不重复)。
阳离子 | H+、Na+、A13+、Ag+、Ba2+ |
阴离子 | OH-、C1-、CO32-、NO3-、SO4- |
已知:
①A、B两溶液呈碱性;C、D、E溶液呈酸性;
②A溶液与E溶液反应既有气体又有沉淀产生;A溶液与C溶液反应只有气体产生;
③D溶液与另外四种溶液反应都能产生沉淀;C只能与D反应产生沉淀;
④上述沉淀包括难溶物和微溶物。
试回答下列问题:
(1)A溶液呈碱性的原因是 (用一个离子方程式表示)。
(2)D溶液是 溶液,E溶液是 溶液(均写化学式)。
(3)写出A溶液与E溶液反应的离子方程式: 。
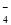 +Cu2S+H+→Cu2++SO2↑+Mn2++H2O(未配平)
+Cu2S+H+→Cu2++SO2↑+Mn2++H2O(未配平)
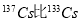 多4个质子
多4个质子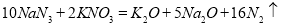 。则下列判断错误的是.
。则下列判断错误的是.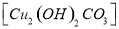 的铜器放入盐酸中浸泡,可除去铜绿
的铜器放入盐酸中浸泡,可除去铜绿