现有一试管NO2,某同学设计如下表实验,以尽可能多地使NO2被水吸收。
⑴请完成下表:
实验步骤 | 实验现象 | 解释(用化学方程式表示) | |
① | 将充满NO2的倒立在盛有水的水槽中,拨去橡皮塞,轻轻晃动试管。 | 试管内气体由 色逐渐变为无色,液面上升至试管高度的 (离管口)处。 |
|
② |
|
|
|
③ | 重复步骤②的操作数次,直至液体充满整个试管。 | 试管内充满无色液体。 | 总反应方程式:
|
⑵在下面方框中画出此实验的装置简图。

下表中的实验操作能达到实验目的或能得出相应结论的是( )
选项 | 实验操作 | 实验目的或结论 |
A | 将混有Ca(OH)2杂质的Mg(OH)2样品,放入水中搅拌成浆状后,加入足量饱和氯化镁溶液充分搅拌、过滤,沉淀用蒸馏水洗涤。 | 除去Mg(OH)2样品中的Ca(OH)2 |
B | 取少量KClO3晶体溶于适量的蒸馏水,再加入硝酸 酸化的AgNO3溶液。 | 检验KC1O3中的氯元素 |
C | 向某溶液中滴加Ba(NO3)2溶液产生白色沉淀,再加稀盐酸沉淀消失。 | 说明原溶液中一定含有CO32-或SO32- |
D | 向盛有1mL 0.01lmol·L-1AgNO3溶液的试管中滴加5滴0.0lmol·L-1NaCl溶液,有白色沉淀生成,再向其中滴加0.01 mol·L-1 NaI溶液,产生黄色沉淀。 | 常温下, Ksp(AgCl)>Ksp(AgI)
|
(15分)已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增加。相关信息如下表所示,根据推断回答下列问题:(答题时A、B、C、D、E用所对应的元素符号表示)
A | A的最高价氧化物对应的水化物化学式为H2AO3 |
B | B元素的第一电离能比同周期相邻两个元素都大 |
C | C原子在同周期原子中半径最大(稀有气体除外),其单质焰色为黄色 |
D | Z的基态原子最外层电子排布式为3s23p2 |
E | E与C位于不同周期,E原子核外最外层电子数与C相同,其余各层电子均充满 |
(1)C在周期表中位于第 周期第 族,E基态原子核外电子排布式是
(2)A、B、D三种元素电负性由大到小排列顺序为 ,其中A的最高价氯化物构成晶体的微粒间作用力为
(3)A和B的最简单氢化物中较稳定的是 (填化学式)。B的最简单氢化物和E的黑色氧化物固体在加热时可反应,写出其反应方程式
(4)E的单质和过氧化氢在稀硫酸中可反应,有人将这个反应设计成原电池,请写出正极反应方程式
(5)煤燃烧产生的烟气中有B的氧化物,会引起严重的环境问题,因此,常用AH4催化还原以消除污染,已知:
① AH4(g)+2 BO2(g)= B2(g)+AO2(g)+2H2O (g) △H1=-867kJ/mol
② 2BO2(g) ? B2O4(g) △H2=-56.9 kJ/mol
写出AH4和B2O4反应的热化学方程式


 =69g/mol时,若n(NO2):n(N2O4)=2:1,
=69g/mol时,若n(NO2):n(N2O4)=2:1,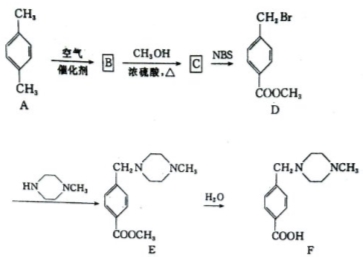
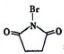 ,则反应C→D的化学方程式为 ,
,则反应C→D的化学方程式为 ,