0 125303 125311 125317 125321 125327 125329 125333 125339 125341 125347 125353 125357 125359 125363 125369 125371 125377 125381 125383 125387 125389 125393 125395 125397 125398 125399 125401 125402 125403 125405 125407 125411 125413 125417 125419 125423 125429 125431 125437 125441 125443 125447 125453 125459 125461 125467 125471 125473 125479 125483 125489 125497 203614
 6LiBr+2H2O+N2↑+4CO2↑其主要工艺流程如下:
6LiBr+2H2O+N2↑+4CO2↑其主要工艺流程如下: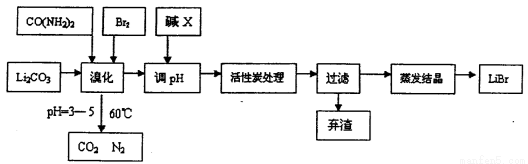
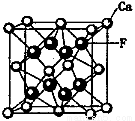
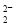 存在,使晶胞沿一个方向拉长,则CaC2晶体中1个C
存在,使晶胞沿一个方向拉长,则CaC2晶体中1个C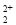 互为等电子体,O
互为等电子体,O
 2NH3(g) △H= -73kJ/mol
2NH3(g) △H= -73kJ/mol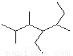 的名称:2,3,5-三甲基-4-乙基庚烷
的名称:2,3,5-三甲基-4-乙基庚烷 K(g)+NaCl(l)
K(g)+NaCl(l)