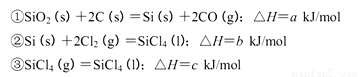0 125239 125247 125253 125257 125263 125265 125269 125275 125277 125283 125289 125293 125295 125299 125305 125307 125313 125317 125319 125323 125325 125329 125331 125333 125334 125335 125337 125338 125339 125341 125343 125347 125349 125353 125355 125359 125365 125367 125373 125377 125379 125383 125389 125395 125397 125403 125407 125409 125415 125419 125425 125433 203614

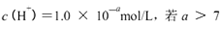 时,则该溶液的pH一定为14-a
时,则该溶液的pH一定为14-a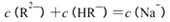
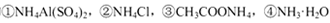 溶液中,c (NH4+)由大到小的顺序是:①>②>③>④
溶液中,c (NH4+)由大到小的顺序是:①>②>③>④ Si3N4(s)+12HCl(g),在温度T0下的2 L密闭容器中,加入0.30 mol SiC14, 0.20 mol N2. 0.36 mol H2进行上述反应,2min后达到平衡,测得固体的质量增加了2.80 g
Si3N4(s)+12HCl(g),在温度T0下的2 L密闭容器中,加入0.30 mol SiC14, 0.20 mol N2. 0.36 mol H2进行上述反应,2min后达到平衡,测得固体的质量增加了2.80 g