下列有关热化学方程式的评价合理的是( )
| 实验事实 | 热化学方程式 | 评价 |
A | 已知H+(aq)+OH-(aq)=H2O(l) △H=-57.3 kJ·mol-1,将稀硫酸与稀氢氧化钡溶液混合 | H2SO4(aq)+Ba(OH)2(aq) =BaSO4(s)+ 2H2O(l) △H=-114.6 kJ·mol-1 | 正确 |
B | 醋酸与稀氢氧化钠溶液混合 | CH3COOH(aq)+NaOH(aq) =CH3COONa(aq)+H2O(l) △H=-57.3kJ·mol-1 | 不正确;因为醋酸状态为“aq”,而不是“l”。 |
C | 160 g SO3气体与适量水恰好完全反应生成H2SO4,放出热量260.6 kJ | SO3(g)+H2O(l)=H2SO4(aq) △H=-130.3 kJ·mol-1 | 不正确;因为反应热为△H=-260.6kJ·mol-1 |
D | 已知25℃、101 kPa下,120g石墨完全燃烧放出热量3935.1 kJ | C(s)+O2(g)=CO2(g) △H=-393.51 kJ·mol-1 | 不正确;同素异形体要注名称:C(石墨) |
下列说法正确的是( )
A.在100 ℃、101 kPa条件下,液态水的气化热为40.69 kJ·mol-1,则H2O(g) H2O(l) 的 ΔH = —40.69 kJ·mol-1
H2O(l) 的 ΔH = —40.69 kJ·mol-1
B.在25℃、101kPa,2mol S的燃烧热是1mol S的燃烧热2倍
C.CH4(g) +2O2(g) = CO2(g) +2H2O(g) ΔH=-akJ·mol-1 ,这里ΔH代表燃烧热
D.已知:
共价键 | C-C | C=C | C-H | H-H |
键能/ kJ·mol-1 | 348 | 610 | 413 | 436 |
则可以计算出反应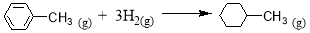 的ΔH为-384 kJ·mol-1
的ΔH为-384 kJ·mol-1
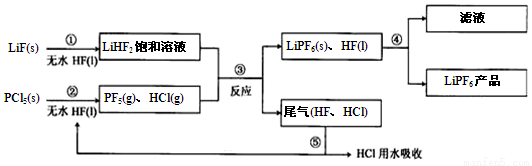
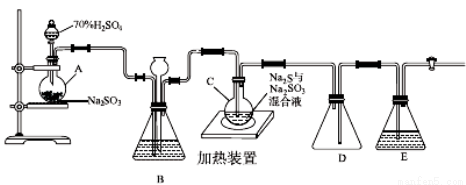
 Na2S2O3(aq) (Ⅲ)
Na2S2O3(aq) (Ⅲ)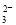 +2H+===S↓+SO2↑+H2O
+2H+===S↓+SO2↑+H2O
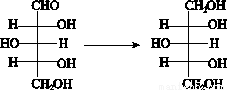
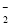 的立体构型是________;R2+的水合离子中,
的立体构型是________;R2+的水合离子中,

 CH2===CHCHO+H2O
CH2===CHCHO+H2O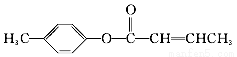 是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为____________________。
是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为____________________。 HCOONa+H2O,下列有关说法不正确的是( )
HCOONa+H2O,下列有关说法不正确的是( ) 