0 12311 12319 12325 12329 12335 12337 12341 12347 12349 12355 12361 12365 12367 12371 12377 12379 12385 12389 12391 12395 12397 12401 12403 12405 12406 12407 12409 12410 12411 12413 12415 12419 12421 12425 12427 12431 12437 12439 12445 12449 12451 12455 12461 12467 12469 12475 12479 12481 12487 12491 12497 12505 203614



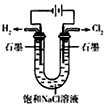
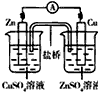

 4SiHCl3(g),达到平衡后,H2与SiHCl3的物质的量浓度分别为0.140mol/L和0.020 mol/L,若H2全部来源于图Ⅱ离子交换膜法的电解产物,理论上需消耗硫酸钾质量为______kg。
4SiHCl3(g),达到平衡后,H2与SiHCl3的物质的量浓度分别为0.140mol/L和0.020 mol/L,若H2全部来源于图Ⅱ离子交换膜法的电解产物,理论上需消耗硫酸钾质量为______kg。 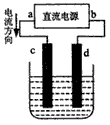
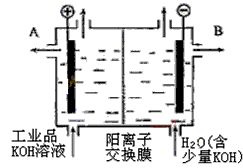
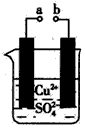
 Cu2O+H2↑。下列说法正确的是
Cu2O+H2↑。下列说法正确的是