0 12228 12236 12242 12246 12252 12254 12258 12264 12266 12272 12278 12282 12284 12288 12294 12296 12302 12306 12308 12312 12314 12318 12320 12322 12323 12324 12326 12327 12328 12330 12332 12336 12338 12342 12344 12348 12354 12356 12362 12366 12368 12372 12378 12384 12386 12392 12396 12398 12404 12408 12414 12422 203614
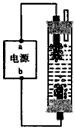
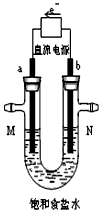
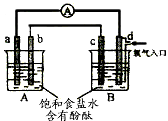
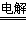 2NaOH+H2↑+Cl2↑ ②H2+Cl2=2HCl
2NaOH+H2↑+Cl2↑ ②H2+Cl2=2HCl
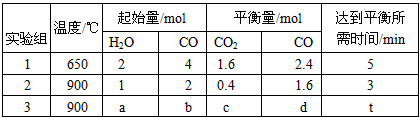
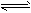 CO2(g) +H2(g),得到如下三组数据
CO2(g) +H2(g),得到如下三组数据