0 12164 12172 12178 12182 12188 12190 12194 12200 12202 12208 12214 12218 12220 12224 12230 12232 12238 12242 12244 12248 12250 12254 12256 12258 12259 12260 12262 12263 12264 12266 12268 12272 12274 12278 12280 12284 12290 12292 12298 12302 12304 12308 12314 12320 12322 12328 12332 12334 12340 12344 12350 12358 203614


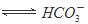 +H+的电离平衡常数 K=____________。(已知:10-5.6=2.5×10-6)。
+H+的电离平衡常数 K=____________。(已知:10-5.6=2.5×10-6)。
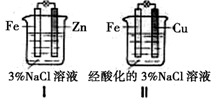
 3Zn(OH)2 +2Fe(OH)3 +4KOH
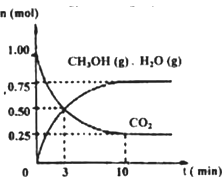
3Zn(OH)2 +2Fe(OH)3 +4KOH CH3OH(g) ΔH1
CH3OH(g) ΔH1  CH3OH(g) + H2O(g) ΔH2
CH3OH(g) + H2O(g) ΔH2