0 11957 11965 11971 11975 11981 11983 11987 11993 11995 12001 12007 12011 12013 12017 12023 12025 12031 12035 12037 12041 12043 12047 12049 12051 12052 12053 12055 12056 12057 12059 12061 12065 12067 12071 12073 12077 12083 12085 12091 12095 12097 12101 12107 12113 12115 12121 12125 12127 12133 12137 12143 12151 203614
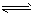 CO2(g)+ H2(g),得到如下三组数据:
CO2(g)+ H2(g),得到如下三组数据: