0 11923 11931 11937 11941 11947 11949 11953 11959 11961 11967 11973 11977 11979 11983 11989 11991 11997 12001 12003 12007 12009 12013 12015 12017 12018 12019 12021 12022 12023 12025 12027 12031 12033 12037 12039 12043 12049 12051 12057 12061 12063 12067 12073 12079 12081 12087 12091 12093 12099 12103 12109 12117 203614
 CH3OH(g)+H2O(g) △H=-49.0 kJ/mol。测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。从反应开始到平衡,氢气的反应速率v(H2)=
CH3OH(g)+H2O(g) △H=-49.0 kJ/mol。测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。从反应开始到平衡,氢气的反应速率v(H2)=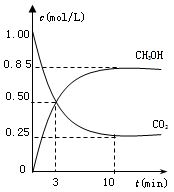


 4CO(g)+BaS(s) ΔH1=571.2 kJ/mol ①
4CO(g)+BaS(s) ΔH1=571.2 kJ/mol ① 2CO2(g)+BaS(s) ΔH2=226.2 kJ/mol ②
2CO2(g)+BaS(s) ΔH2=226.2 kJ/mol ②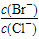 =________。
=________。  2CO(g)的ΔH3=____kJ/mol。
2CO(g)的ΔH3=____kJ/mol。 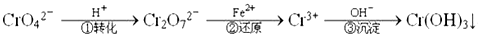
 Cr2O72-(橙色)+H2O
Cr2O72-(橙色)+H2O  Cr3+(aq)+3OH-(aq) 常温下,Cr(OH)3的溶度积Ksp=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至_____。
Cr3+(aq)+3OH-(aq) 常温下,Cr(OH)3的溶度积Ksp=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至_____。