一元弱酸HA(aq)中存在下列电离平衡:HA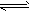 A-+H+。将1.0 mol HA分子加入1.0 L水中,下图中,表示溶液中HA、H+、A-的物质的量浓度随时间而变化的曲线正确的是
A-+H+。将1.0 mol HA分子加入1.0 L水中,下图中,表示溶液中HA、H+、A-的物质的量浓度随时间而变化的曲线正确的是
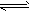 A-+H+。将1.0 mol HA分子加入1.0 L水中,下图中,表示溶液中HA、H+、A-的物质的量浓度随时间而变化的曲线正确的是
A-+H+。将1.0 mol HA分子加入1.0 L水中,下图中,表示溶液中HA、H+、A-的物质的量浓度随时间而变化的曲线正确的是 [ ]
A.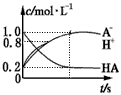
B.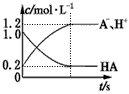
C.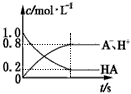
D.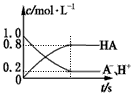

B.

C.

D.

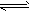 A-+H+。将1.0 mol HA分子加入1.0 L水中,下图中,表示溶液中HA、H+、A-的物质的量浓度随时间而变化的曲线正确的是
A-+H+。将1.0 mol HA分子加入1.0 L水中,下图中,表示溶液中HA、H+、A-的物质的量浓度随时间而变化的曲线正确的是 


