0 110385 110393 110399 110403 110409 110411 110415 110421 110423 110429 110435 110439 110441 110445 110451 110453 110459 110463 110465 110469 110471 110475 110477 110479 110480 110481 110483 110484 110485 110487 110489 110493 110495 110499 110501 110505 110511 110513 110519 110523 110525 110529 110535 110541 110543 110549 110553 110555 110561 110565 110571 110579 203614
 2X(g)+Y(g)
2X(g)+Y(g) 3R(g),该反应经2s后达到平衡,测得R气体的浓度为0.6mol/L。下列说法中错误的是( )
3R(g),该反应经2s后达到平衡,测得R气体的浓度为0.6mol/L。下列说法中错误的是( ) 达到平衡时,下列说法中正确的是( )
达到平衡时,下列说法中正确的是( ) xC(g),△H<0;在2min时反应达到平衡状态(温度不变)剩余了0.8molB,并测得C的浓度为0.4mol·L—1,请填写下列空白:
xC(g),△H<0;在2min时反应达到平衡状态(温度不变)剩余了0.8molB,并测得C的浓度为0.4mol·L—1,请填写下列空白: 3)若继续向原平衡混合物的容器中通入少量氦气(假设氦气和A、B、C都不反应)后,化学平衡(填字母) 。
3)若继续向原平衡混合物的容器中通入少量氦气(假设氦气和A、B、C都不反应)后,化学平衡(填字母) 。 C(g)+D(g) 已达到反应限度的是
C(g)+D(g) 已达到反应限度的是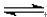 2HBr(g),此反应达到平衡的标志是
2HBr(g),此反应达到平衡的标志是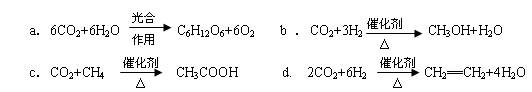
 CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H=-49.0kJ/mol
CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H=-49.0kJ/mol


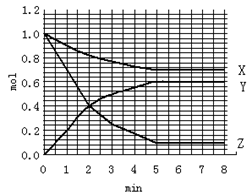
 2C(g),下列说法属于该反应达到平衡标志的是( )
2C(g),下列说法属于该反应达到平衡标志的是( )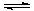 2NH3,下列有关说法错误的是
2NH3,下列有关说法错误的是