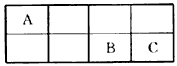
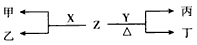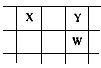| J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如右表;J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的金属元素。 | |||||||||||||||
 | |||||||||||||||
| (1)M的离子结构示意图为______;元素T在周期表中位于周期表_________;J和R的最高价氧化物对应的水化物的酸性较强的是_______(写化学式)。 (2)M和T形成的化合物在潮湿的空气中冒白色烟雾,反应的化学方程式为_________。 (3)L的最简单气态氢化物甲的水溶液显碱性。 一定条件下,甲在固定体积的密闭容器中发生分解反应(△H>0)并达平衡后,仅改变下表中反应条件x,该平衡体系中随x递增y递减的是____(选填序号)。 | |||||||||||||||
| |||||||||||||||
|
(4)R所在族2 ~ 5周期元素单质分别与H2反应生成l mol气态氢化物的反应热如下,表示生成1 mol硒化氢反应热的是__________(填字母代号)。 |
 Cu2+(aq)+2OH-(aq), Ksp=2×10-20]
Cu2+(aq)+2OH-(aq), Ksp=2×10-20]  2EC3 (g),△H= -196. 6 kJ mol-1。平衡时容器内气体压强为起始时的90%。
2EC3 (g),△H= -196. 6 kJ mol-1。平衡时容器内气体压强为起始时的90%。
 H=-283.0 kJ·mol-1
H=-283.0 kJ·mol-1  H=-296.0 kJ·mol-1
H=-296.0 kJ·mol-1