0 103635 103643 103649 103653 103659 103661 103665 103671 103673 103679 103685 103689 103691 103695 103701 103703 103709 103713 103715 103719 103721 103725 103727 103729 103730 103731 103733 103734 103735 103737 103739 103743 103745 103749 103751 103755 103761 103763 103769 103773 103775 103779 103785 103791 103793 103799 103803 103805 103811 103815 103821 103829 203614

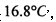 沸点是
沸点是 )
)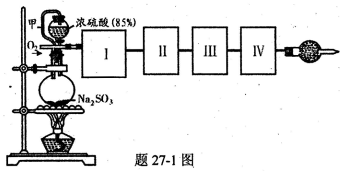
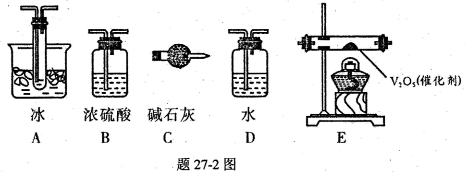
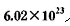 个电子转移,则该反应的化学方程式为__________________
个电子转移,则该反应的化学方程式为__________________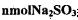 粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2 —段时间后,测得装置IV增重了 mg,则实验中SO2的转化率为__________________.(用含m、n的代数式填写)
粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2 —段时间后,测得装置IV增重了 mg,则实验中SO2的转化率为__________________.(用含m、n的代数式填写) 有关的是( )[
有关的是( )[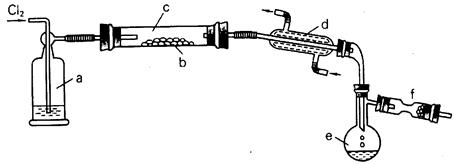
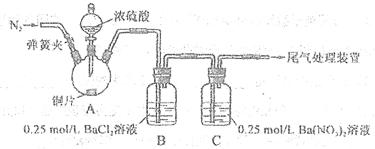
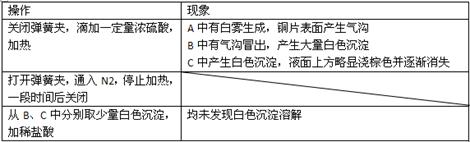
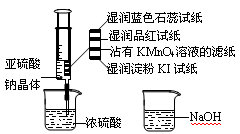

 。
。 量的测量结果比实际值________(填“偏高”、“偏低”或“没影响”)。
量的测量结果比实际值________(填“偏高”、“偏低”或“没影响”)。