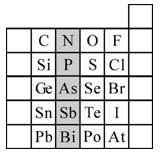
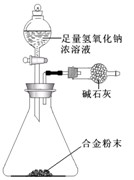
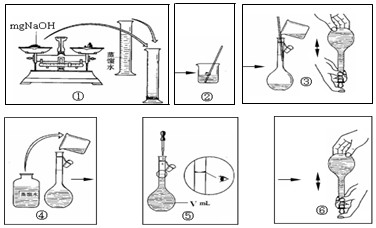
0 102675 102683 102689 102693 102699 102701 102705 102711 102713 102719 102725 102729 102731 102735 102741 102743 102749 102753 102755 102759 102761 102765 102767 102769 102770 102771 102773 102774 102775 102777 102779 102783 102785 102789 102791 102795 102801 102803 102809 102813 102815 102819 102825 102831 102833 102839 102843 102845 102851 102855 102861 102869 203614