题目内容
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、18gH2O含有10 NA个质子 |
| B、1mol己烷含有18NA个化学键 |
| C、22.4L氨水含有NA个NH3分子 |
| D、56g铁片投入足量浓H2SO4中生成NA个SO2分子 |
考点:阿伏加德罗常数
专题:
分析:A.水分子中含有10个质子,1mol水中含有10mol质子;
B.己烷中含有19个化学键,1mol己烷含有19NA个化学键;
C.标准状况下氨水不是气体,不能使用标况下的气体摩尔体积计算氨水的物质的量;
D.铁与浓硫酸发生钝化,阻止了反应的继续进行,无法计算生成的二氧化硫的物质的量.
B.己烷中含有19个化学键,1mol己烷含有19NA个化学键;
C.标准状况下氨水不是气体,不能使用标况下的气体摩尔体积计算氨水的物质的量;
D.铁与浓硫酸发生钝化,阻止了反应的继续进行,无法计算生成的二氧化硫的物质的量.
解答:
解:A.18水的物质的量为1mol,1mol水中含有10mol质子,含有10NA个质子,故A正确;
B.己烷中含有19个化学键,1mol己烷含有19NA个化学键,故B错误;
C.标况下,氨水不是气体,题中条件无法计算氨气的物质的量,故C错误;
D.56g铁的物质的量为1mol,由于铁与浓硫酸能够发生钝化,阻止了反应的进行,无法计算反应生成二氧化硫的物质的量,故D错误;
故选A.
B.己烷中含有19个化学键,1mol己烷含有19NA个化学键,故B错误;
C.标况下,氨水不是气体,题中条件无法计算氨气的物质的量,故C错误;
D.56g铁的物质的量为1mol,由于铁与浓硫酸能够发生钝化,阻止了反应的进行,无法计算反应生成二氧化硫的物质的量,故D错误;
故选A.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确标况下气体摩尔体积的使用条件,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系;试题有利于提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
部分弱酸的电离平衡常数如表:下列说法正确的是( )
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | Ki=1.77×10-4 | Ki=4.9×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
| A、0.1 mol?L-lNaHCO3溶液中各离子浓度的大小顺序为:c( Na+)>c(HCO3-)c(HJ-)>c(OH-) |
| B、少量的CO2通人到NaCN溶液中:CN-+H2O+CO2═HCN+HCO3- |
| C、用0.1 mol?L-l NaOH溶液中和等浓度的HCN溶液和HCOOH溶液时,前者所需NaOH溶液体积大 |
| D、相同体积的0.1 mol?L-l HCOONa溶液比0.1 mol?L-l NaCN溶液所含离子总数小 |
设NA 为阿伏加德罗常数的值,下列叙述正确的是( )
| A、88.0g 干冰中含有的电子数为8.0NA |
| B、常温下,11.2 L 乙烯在氧气中完全燃烧转移的电子数为6.0NA |
| C、常温下1.0 L 0.1 mol?L-1NH4Cl 溶液中,NH4+和H+总数大于0.1NA |
| D、1.2g 金刚石中含有的碳碳键数为0.4 NA |
 一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):
一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO): 按要求对图中两极进行必要的联接并填空:
按要求对图中两极进行必要的联接并填空: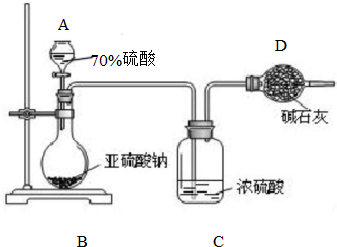 为测定某亚硫酸钠样品的纯度,甲同学称取10.0g固体,进行如下实验:
为测定某亚硫酸钠样品的纯度,甲同学称取10.0g固体,进行如下实验: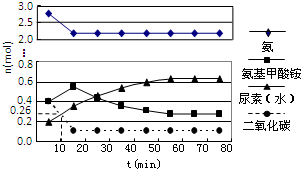 尿素(H2NCONH2)是一种非常重要的高氮化肥,工业上合成尿素的反应分为如下两步:
尿素(H2NCONH2)是一种非常重要的高氮化肥,工业上合成尿素的反应分为如下两步: