题目内容
17.依据以下化学反应漫画情景进行判断,下列有关说法不正确的是( )
| A. | 此反应不可能是复分解反应 | |
| B. | 若金属1是锌,则金属2可能是铁 | |
| C. | 还原性:金属1>金属2 | |
| D. | 若金属2是铜,则生成2 mol铜时反应过程中转移2 mol电子 |
分析 A、此反应是单质和化合物反应生成新的单质和新的化合物的过程;
B、锌比铁活泼,即锌可以将亚铁离子从此可溶性的盐溶液中置换出来;
C、活泼性强的置换活泼性弱的;
D、生成1mol铜转移2mol的电子.
解答 解:A、此反应是单质和化合物反应生成新的单质和新的化合物的过程,是置换反应,而不是复分解反应,故A正确;
B、锌比铁活泼,即锌可以将亚铁离子从此可溶性的盐溶液中置换出来,则金属1是锌,金属2可能是铁,故B正确;
C、活泼性强的置换活泼性弱的,所以还原性:金属1>金属2,故C正确;
D、生成1mol铜转移2mol的电子,所以生成2 mol铜时反应过程中转移4 mol电子,故D错误;
故选D.
点评 本题考查金属的活泼性、反应的类型和电子转移的数目,综合性强,但比较容易,学生要知道氧化还原反应中还原剂的还原性强于还原产物的还原性.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
7.下列图示与对应的叙述相符的是( )
| A. | 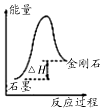 如图所示,从能量角度考虑,石墨比金刚石稳定 | |
| B. | 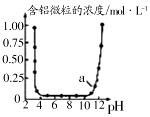 图表示Al3+与OH-反应时含铝微粒浓度变化曲线,图中a点溶液中大量存在Al3+ | |
| C. | 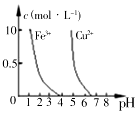 如图所示,若除去CuSO4溶液中的Fe3+,可向溶液中加入适量NaOH溶液,调节pH≈4 | |
| D. | 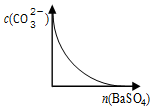 如图所示,在饱和Na2CO3溶液中逐步加BaSO4固体后,溶液中c(CO32-)的变化 |
5.下列有关热化学方程式及其叙述正确的是( )
| A. | 氢气的燃烧热为285.5 kJ•mol-1,则水分解的热化学方程式为2H2O(l)═2H2(g)+O2(g)△H=+285.5 kJ•mol-1 | |
| B. | 已知2C(石墨,s)+O2(g)═2CO(g)△H=-221 kJ•mol-1,则石墨的燃烧热为 110.5 kJ•mol-1 | |
| C. | 已知N2(g)+3H2(g)?2NH3(g)△H=-92.4 kJ•mol-1,则在一定条件下将1 mol N2和3 mol H2置于一密闭容器中充分反应后最多可放出92.4 kJ的热量 | |
| D. | 已知乙醇和乙烯的燃烧热分别为1 366.8 kJ•mol-1和1 411.0 kJ•mol-1,则乙烯水化制乙醇的热化学方程式为C2H4(g)+H2O(l)═C2H5OH(l)△H=-44.2 kJ•mol-1 |
2.常温下,用0.1mol/L的盐酸滴定a mL NaOH稀溶液.反应恰好完全时,消耗盐酸b mL.此时溶液时中c (OH-)是( )
| A. | 1.0×10-7 mol/L | B. | 1.0×107 mol/L | C. | $\frac{0.1}{a}$mol/L | D. | $\frac{0.1b}{a+b}$mol/L |
9.高铁酸钾(K2FeO4)是一种既能杀菌、消毒,又能絮凝净水的水处理剂.工业制备高铁酸钾反应的离子方程式为:Fe(OH)3+ClO-+OH-→FeO42-+Cl-+H2O(未配平)下列有关说法不正确的是( )
| A. | 由上述反应可知,ClO-的氧化性强于FeO42- | |
| B. | 高铁酸钾中铁显+6价 | |
| C. | 上述反应中氧化剂和还原剂的物质的量之比为2:3 | |
| D. | K2FeO4处理水时,不仅能消毒杀菌,而且生成的Fe3+水解形成Fe(OH)3胶体能吸附水中的悬浮杂质 |
6.化学与人类生活、生产、环境密切相关,下列有关说法不正确的是( )
| A. | 雾霾可能是许多细小液体小液滴和固体小颗粒分散到空气中形成的一种胶体 | |
| B. | 我国神七宇航员所穿航天服主要成分是由碳化硅、陶瓷和碳纤维复合而成的,它是一种新型有机高分子材料 | |
| C. | “84”消毒液主要成分为次氯酸钠,与适量白醋混合使用消毒效果会更好 | |
| D. | 夏季马路喷洒氯化钙溶液,氯化钙跟水分子结合形成结晶水合物起到保湿作用 |
 .
.