题目内容
已知A~H以及X、Y的转化关系如图:

(1)电解上述滤液时产生G的电极是 .其电极反应式为 .
(2)取图中滤液做焰色反应显紫色,图中焰色反应显紫色的还有 .
(3)写出黑色固体与X浓溶液共热反应的离子方程式 .
(4)写出G与B溶液反应的化学方程式 .

(1)电解上述滤液时产生G的电极是
(2)取图中滤液做焰色反应显紫色,图中焰色反应显紫色的还有
(3)写出黑色固体与X浓溶液共热反应的离子方程式
(4)写出G与B溶液反应的化学方程式
考点:无机物的推断
专题:推断题
分析:无色液体E可猜想为水,利用滤液进行焰色反应实验显紫色,则滤液中含有钾离子,且电解滤液得到的产物中有两种气体和一种溶液,可猜想滤液为KCl溶液,则Y是KOH,气体G能与B反应生成无色气体C,比较氯气、氢气的性质,可猜想G是Cl2,H是H2,则X溶液为盐酸,B为H2O2,氯气和双氧水溶液反应生成盐酸和氧气,再结合转化关系可得A是MnO2,D是KClO3,E是H2O,将猜想的物质代入转化关系中进行验证,所得结论完全正确,以此解答该题.
解答:
解:无色液体E可猜想为水,利用滤液进行焰色反应实验显紫色,则滤液中含有钾离子,且电解滤液得到的产物中有两种气体和一种溶液,可猜想滤液为KCl溶液,则Y是KOH,气体G能与B反应生成无色气体C,比较氯气、氢气的性质,可猜想G是Cl2,H是H2,则X溶液为盐酸,B为H2O2,氯气和双氧水溶液反应生成盐酸和氧气,再结合转化关系可得A是MnO2,D是KClO3,E是H2O,
(1)G是氯气,电解氯化钾溶液时,阳极上氯离子放电生成氯气,电极反应式为:2Cl--2e-=Cl2↑,故答案为:阳极;2Cl--2e-=Cl2↑;
(2)钾元素的焰色反应显紫色,所以氯酸钾、氢氧化钾和氯化钾的焰色反应都显紫色,即D、F、Y的焰色反应都显紫色,故答案为:D、F、Y;
(3)黑色固体A是二氧化锰,X是盐酸,在加热条件下,二氧化锰和浓盐酸反应生成氯化锰、氯气和水,离子反应方程式为:MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O,故答案为:MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O;
(4)G是氯气,B是双氧水,氯气和双氧水反应生成氯化氢和氧气,反应方程式为:Cl2+H2O2=O2↑+2HCl,故答案为:Cl2+H2O2=O2↑+2HCl.
(1)G是氯气,电解氯化钾溶液时,阳极上氯离子放电生成氯气,电极反应式为:2Cl--2e-=Cl2↑,故答案为:阳极;2Cl--2e-=Cl2↑;
(2)钾元素的焰色反应显紫色,所以氯酸钾、氢氧化钾和氯化钾的焰色反应都显紫色,即D、F、Y的焰色反应都显紫色,故答案为:D、F、Y;
(3)黑色固体A是二氧化锰,X是盐酸,在加热条件下,二氧化锰和浓盐酸反应生成氯化锰、氯气和水,离子反应方程式为:MnO2+4H++2Cl-
| ||
| ||
(4)G是氯气,B是双氧水,氯气和双氧水反应生成氯化氢和氧气,反应方程式为:Cl2+H2O2=O2↑+2HCl,故答案为:Cl2+H2O2=O2↑+2HCl.
点评:本题考查元素化合物的特性和反应,为高频考点,用框图设问可以考查学生正向思维、逆向思维、发散和收敛思维,能根据题眼正确判断化合物是解本题的关键,难度中等.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
目前市场上销售的强生、妙思乐及帮宝适等婴儿卫浴产品常常标有“温和”、“纯净”等字样,但其中却含有甲醛以及1,4-二氧杂环乙烷等有害物质.1,4-二氧杂环乙烷的结构简式为 ,下列有关其性质的叙述正确的是( )
,下列有关其性质的叙述正确的是( )
 ,下列有关其性质的叙述正确的是( )
,下列有关其性质的叙述正确的是( )| A、1,4-二氧杂环乙烷与丁酸互为同分异构体 |
| B、1,4-二氧杂环乙烷与乙酸乙酯互为同系物 |
| C、1,4-二氧杂环乙烷与钠反应可放出氢气 |
| D、1,4-二氧杂环乙烷的分子中所有原子不可能共平面 |
目前国家仍允许在面粉中添加过氧化苯甲酰来使面粉增白,但它的安全性已引起公众质疑.已知过氧化苯甲酰能发生如下反应:
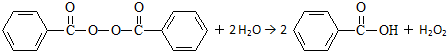
下列叙述不正确的是( )
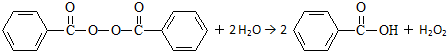
下列叙述不正确的是( )
| A、并非在食品中添加化学物质都对人体有害 |
| B、过氧化苯甲酰能使面粉增白的原因是它与水反应生成的H2O2具有漂白性 |
| C、苯甲酸的同分异构体中,既属于醛又属于酚的物质有4种 |
| D、甲苯经两步取代反应和两步催化氧化反应可转化为苯甲酸 |
向某密闭容器中充入1mol CO和2mol H2O(g),发生反应:CO(g)+H2O(g)
CO2(g)+H2(g);当反应达到平衡时,CO的体积分数为x.若维持容器的体积和温度不变,超始物质按下列四种配比充入该容器中,达到平衡时CO的体积分数大于x的是( )
| ||
| 高温 |
| A、0.5 mol CO+1.5 mol H2O(g)+0.4 mol CO2+0.4 mol H2 |
| B、1 mol CO+1 mol H2O(g)+1 mol CO2+1 mol H2 |
| C、0.5 mol CO+2 mol H2O(g)+1 mol CO2+1 mol H2 |
| D、0.5 mol CO+1.5 mol H2O(g)+0.5 mol CO2+0.5 mol H2 |
pH相同的NaOH溶液和氨水,分别用蒸馏水稀释原体积的m和n倍,若稀释后两溶液的pH仍然相同,则m和n的关系是( )
| A、m>n | B、m<n |
| C、m=n | D、不能确定 |
汽油燃烧产生的汽车尾气中,所含主要气体污染物之一的是( )
| A、可吸入颗粒物 |
| B、硫的氧化物 |
| C、磷的氧化物 |
| D、碳的氧化物 |
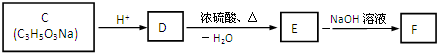
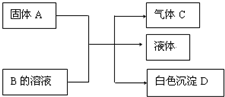 A、B、C、D均为中学化学常见的物质,其组成元素均为主族元素.它们间的反应关系如下图所示.(除(2)外,反应均在常温下进行)
A、B、C、D均为中学化学常见的物质,其组成元素均为主族元素.它们间的反应关系如下图所示.(除(2)外,反应均在常温下进行)