题目内容
19.下列离子方程式或化学反应方程式与所述事实相符且正确的是( )| A. | 稀硫酸滴在铜片上:Cu+2H+=Cu2++H2 | |
| B. | 向20mL0.5mol•L-1FeBr2溶液中通入224mL Cl2(标准状况):2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- | |
| C. | Ca(HCO3)2与过量Ca(OH)2溶液反应:Ca2++HCO3-+2OH-═CaCO3↓+CO32-+2H2O | |
| D. | NH4Al(SO4)2溶液中加入Ba(OH)2溶液至恰好使SO42-完全沉淀:Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O |
分析 A、铜和稀硫酸不反应;
B、二价铁离子还原性强于溴离子,氯气少量先反应二价铁离子;
C、Ca(HCO3)2与过量Ca(OH)2溶液反应时,设Ca(HCO3)2的物质的量为1mol,据此分析消耗的氢氧化钙的物质的量;
D、向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰好使SO42-完全沉淀,说明SO42-与Ba2+的比例是1:2.
解答 解:A、铜和稀硫酸不反应,不能置换出氢气,故A错误;
B、向20mL0.5mol•L-1FeBr2溶液中通入224mL Cl2(标准状况),离子方程式2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl-,故B正确;
C、Ca(HCO3)2与过量Ca(OH)2溶液反应时,设Ca(HCO3)2的物质的量为1mol,故消耗氢氧化钙中的2molOH-和1molCa2+,反应生成2mol碳酸钙和2mol水,离子方程式为Ca2++OH-+HCO3-=CaCO3↓+H2O,故C错误;
D、向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰好使SO42-完全沉淀,离子方程式为:2Ba2++NH4++Al3++2SO42-+4OH-═Al(OH)3↓+NH3•H2O+2BaSO4↓,故D错误;
故选B.
点评 本题考查了离子方程式书写,侧重考查复分解、氧化还原反应的离子方程式书写,明确反应实质是解题关键,注意可逆反应不能进行到底,注意反应物用量对反应产物的影响,题目难度中等.

练习册系列答案
相关题目
10.下列说法或表示法不正确的是( )
| A. | 从C(石墨)=C(金刚石)△H=1.9 kJ•mol-1,可知金刚石比石墨更稳定 | |
| B. | 已知2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ/mol,则H2的燃烧热为285.8 kJ/mol | |
| C. | 在稀溶液中:H++OH-═H2O△H=-57.3kJ•mol-1,若将含1mol CH3COOH的醋酸溶液与含1 mol Ba(OH)2的溶液混合,放出的热量小于57.3 kJ | |
| D. | 图中a曲线表示合成氨(放热反应)使用催化剂时,反应过程中的能量变化 |
8.下列离子方程式书写正确的是( )
| A. | 氢氧化钡与稀硫酸反应:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| B. | Al2O3溶于盐酸中:O2-+2H+═H2O | |
| C. | 氯化铝溶液中加入少量氨水:Al3++3OH-═Al(OH)3↓ | |
| D. | Cu(OH)2中加入硝酸:Cu(OH)2+2H+═Cu2++2H2O |
9.下列离子中半径最小的是( )
| A. | F- | B. | Cl- | C. | Na+ | D. | Mg2+ |
 实验室用如图所示装置制备乙酸乙酯.
实验室用如图所示装置制备乙酸乙酯.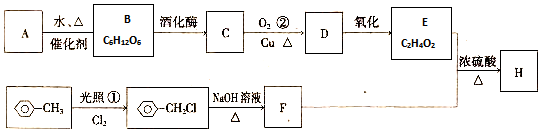
 ,
,