题目内容
下列关于外围电子排布式为3s23p4的粒子描述正确的是( )
| A、它的原子核外有三种形状不同的电子云 |
| B、它的原子核外电子共有16种不同的运动状态 |
| C、它的元素符号为O |
D、核外电子轨道表示式为 |
考点:原子核外电子排布
专题:原子组成与结构专题
分析:A.电子云的形状种数由该原子能级种类确定;
B.原子核外电子运动状态和该原子的核外电子数相等;
C.价电子构型为3s23p4的元素是16号元素S;
D.3p能级上电子排布图违反洪特规则.
B.原子核外电子运动状态和该原子的核外电子数相等;
C.价电子构型为3s23p4的元素是16号元素S;
D.3p能级上电子排布图违反洪特规则.
解答:
解:A.价电子构型为3s23p4的元素是16号元素S,具有s和p两种能级,因此该原子的电子云形状有两种,故A错误;
B.S原子具有16个核外电子,处于不同能层、能级上的电子具有的能量不同,同一能级上的电子自旋方向相反,故有16种不同的运动状态,故B正确;
C.价电子构型为3s23p4的元素是16号元素S,氧元素的价电子构型为:2s22p4,故C错误;
D.当电子排布在同一能级的不同轨道时,总是优先单独占据一个轨道,且自旋方向相同,所以3p能级上电子排布图违反洪特规则,故D错误;
故选:B.
B.S原子具有16个核外电子,处于不同能层、能级上的电子具有的能量不同,同一能级上的电子自旋方向相反,故有16种不同的运动状态,故B正确;
C.价电子构型为3s23p4的元素是16号元素S,氧元素的价电子构型为:2s22p4,故C错误;
D.当电子排布在同一能级的不同轨道时,总是优先单独占据一个轨道,且自旋方向相同,所以3p能级上电子排布图违反洪特规则,故D错误;
故选:B.
点评:本题考查原子核外电子排布,明确构造原理、洪特规则等知识点是解本题关键,难度不大.

练习册系列答案
相关题目
下列各物质中,互为同系物的是( )
| A、CHCl3和氯乙烷 |
| B、HCOOCH3和CH3COOH |
C、 和 和 |
D、 和 和 |
原电池电极的“正”与“负”不仅与电极材料的性质有关,也与电解质溶液有关.下列说法中正确的是( )
| A、由Fe、Cu和FeCl3溶液组成的原电池中,负极反应式为:Cu-2e-═Cu2+ |
| B、由Al、Cu和稀硫酸组成的原电池中,负极反应式为:Cu-2e-═Cu2+ |
| C、由Al、Mg和NaOH溶液组成的原电池中,负极反应:Al+4OH--3e-═AlO2-+2H2O |
| D、由Al、Cu和浓HNO3溶液组成的原电池中,负极反应式为:Al-3e-═Al3+ |
已知化学反应A2(g)+B2(g)═2AB(g)的能量变化如图所示,下列叙述中正确的是( )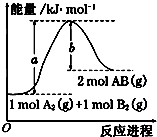

| A、该反应热△H=-(a-b) kJ?mol-1 |
| B、每生成2mol AB(g)吸收b kJ |
| C、该反应中反应物的总能量高于生成物的总能量 |
| D、该反应中反应物的总键能大于生成物的总键能 |
下列分子中所有的原子都满足最外层为8电子结构的是( )
| A、BCl3 |
| B、PCl3 |
| C、SF6 |
| D、SiH4 |
下列说法正确的是( )
| A、凡是金属元素跟非金属元素化合都形成离子化合物 |
| B、共价化合物只含有共价键,离子化合物也只含有离子键 |
| C、离子化合物中,一个阴离子可同时与多个阳离子之间有静电作用 |
| D、溶于水可以导电的化合物一定是离子化合物 |
有一种燃料电池,所用燃料为H2和空气,电解质为熔融的K2CO3.电池的总反应式为2H2+O2=2H2O,负极反应为H2+CO32--2e-=H2O+CO2.该电池放电时,下列说法中正确的( )
| A、正极反应为2H2O+O2+4e-=4OH- |
| B、CO32-向负极移动 |
| C、电子由正极经外电路流向负极 |
| D、电池中CO32-的物质的量将逐渐减少 |