题目内容
在容积不变的密闭容器中,一定条件下发生反应:2A?B(g)+2C(g),且达到平衡.当升高温度时气体的密度增大,则下列叙述中正确的是( )
| A、升高温度,平衡一定逆向移动 |
| B、若正反应是放热反应,则A为气态 |
| C、物质A一定为非气态,且正反应是吸热反应 |
| D、A可能为气态或非气态 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:达到化学平衡后,升高温度,容器内气体的密度增大,说明气体的质量增大,要使气体的密度增大,根据ρ=
知,A一定为非气态,对于容器体积固定的可逆反应,惰性气体不影响平衡的移动,但温度一定影响反应速率.
| m |
| M |
解答:
解:A.反应可能是吸热反应或放热反应,升高温度,正逆反应速率都增大,平衡向吸热反应方向发生移动,故A错误;
B.若正反应是放热反应,升高温度平衡向逆反应方向移动,容器内气体的密度增大,说明气体的质量增大,A为气体,密度不变,A为非气态,密度减小,故B错误;
C.因为容器的体积固定,如果A是气体,升高温度时,无论平衡向哪方向移动,气体的密度始终不变,则A一定是非气体,且升高温度,平衡向正反应方向移动时气体的密度才增大,所以正反应是吸热反应,故C正确;
D.由题意A一定为非气态,升高温度气体的密度增大,一定正向移动,反应吸热,若A为气体.密度反应过程中不变,故D错误;
故选C.
B.若正反应是放热反应,升高温度平衡向逆反应方向移动,容器内气体的密度增大,说明气体的质量增大,A为气体,密度不变,A为非气态,密度减小,故B错误;
C.因为容器的体积固定,如果A是气体,升高温度时,无论平衡向哪方向移动,气体的密度始终不变,则A一定是非气体,且升高温度,平衡向正反应方向移动时气体的密度才增大,所以正反应是吸热反应,故C正确;
D.由题意A一定为非气态,升高温度气体的密度增大,一定正向移动,反应吸热,若A为气体.密度反应过程中不变,故D错误;
故选C.
点评:本题考查化学平衡的影响因素,题目难度中等,解答本题的关键是容器密度的变化,答题时注意体会.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
下列操作错误的是( )(填序号)
| A、用蒸发皿进行加热蒸发实验时,不垫石棉网 |
| B、浓硫酸不慎沾到皮肤上,迅速用NaOH溶液清洗,再用水洗 |
| C、蒸馏时,将温度计水银球插入液面以下 |
| D、闻气体气味时,用手在容器口轻轻扇动,使少量气体飘入鼻孔中 |
| E、使用分液漏斗和容量瓶时,首先检查是否漏水 |
对实验Ⅰ~Ⅳ的实验现象判断正确的是( )
A、 实验Ⅰ:产生红褐色沉淀 |
B、 实验Ⅱ:试管中溶液变红色 |
C、 实验Ⅲ:试管中溶液变红色 实验Ⅲ:试管中溶液变红色 |
D、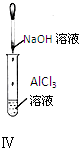 实验Ⅳ:试管中先出现白色沉淀,后溶解 |
关于0.1mol?L-1 NH4Cl溶液,下列说法正确的是( )
| A、c(Cl-)>c(H+)>c(NH4+)>c(OH-) |
| B、c(H+)=c(NH3?H2O)+c(OH-) |
| C、加水稀释,溶液中所有离子的浓度均减小 |
| D、向溶液中加入少量CH3COONa固体,NH4+的水解程度增大 |
下列化学式一定表示一种物质的是( )
| A、CF2Cl2 |
| B、C6H12O6 |
| C、C12H22O11 |
| D、C2H4O2 |
采用以下措施一定会使一个平衡体系发生移动的是( )
| A、加入一种反应物 |
| B、对平衡体系增加压强 |
| C、改变温度 |
| D、使用催化剂 |
阿伏加德罗常数约为6.02×1023mol-1,下列叙述正确的是( )
| A、常温常压下,18.0g重水(D2O)所含的电子数约为10×6.02×1023 |
| B、2.24LCl2中含有的原子数为0.2×6.02×1023 |
| C、室温下,42.0g乙烯和丙烯的混合气体中含有的碳原子数约为3×6.02×1023 |
| D、7.8g过氧化钠粉末与水反应转移的电子数为0.1×6.02×1023 |
 如图是部分短周期元素的单质及其化合物(或其溶液)的转化关系,已知在常温常压下,A是固体,B、C、D、E是非金属单质且都是气体;C呈黄绿色;F是淡黄色的化合物;化合物G的焰色反应为黄色,化合物I和J通常状况下呈气态;J能使湿润的红色石蕊试纸变蓝.
如图是部分短周期元素的单质及其化合物(或其溶液)的转化关系,已知在常温常压下,A是固体,B、C、D、E是非金属单质且都是气体;C呈黄绿色;F是淡黄色的化合物;化合物G的焰色反应为黄色,化合物I和J通常状况下呈气态;J能使湿润的红色石蕊试纸变蓝.