题目内容
海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等.
(1)在光照条件下,氯气和氢气反应过程如下:
①Cl2→Cl+Cl ②Cl+H2→HCl+H ③H+Cl2→HCl+Cl …
反应②中形成的化合物的电子式为 ;反应③中被破坏的化学键属于 键(填“极性”或“非极性”)
(2)已知在短周期主族元素中,元素A与氯元素相邻且属同一周期,元素B也与氯元素相邻且属于同一主族,那么比较元素A、B以及氯元素三者的原子半径由大到小的顺序是 (用元素符号表示).与氯元素同周期且金属性最强的元素位于周期表的第 周期 族.
(3)卤素单质及化合物在许多性质上都存在着递变规律.下列有关说法错误的是 (填字母).
a.卤素单质的熔沸点按F2、Cl2、Br2、I2的顺序由低到高
b.原子半径按F、Cl、Br、I的顺序由大到小
c.卤素单质的稳定性按HF、HCl、HBr、HI的顺序由强到弱
d.卤素单质与氢气化合按F2、Cl2、BR2、I2的顺序由难变易
e.最外层电子数按F、Cl、Br、I的顺序由少到多
(4)碘单质及其化合物具有重要应用.下列说法正确的是 (填字母).
a.
I与
I互为同位素
b.加碘食盐能使淀粉溶液变蓝
c.从海带食盐提取I2的过程只发生化学变化
d.提纯含沙的粗碘可用升华法.
(1)在光照条件下,氯气和氢气反应过程如下:
①Cl2→Cl+Cl ②Cl+H2→HCl+H ③H+Cl2→HCl+Cl …
反应②中形成的化合物的电子式为
(2)已知在短周期主族元素中,元素A与氯元素相邻且属同一周期,元素B也与氯元素相邻且属于同一主族,那么比较元素A、B以及氯元素三者的原子半径由大到小的顺序是
(3)卤素单质及化合物在许多性质上都存在着递变规律.下列有关说法错误的是
a.卤素单质的熔沸点按F2、Cl2、Br2、I2的顺序由低到高
b.原子半径按F、Cl、Br、I的顺序由大到小
c.卤素单质的稳定性按HF、HCl、HBr、HI的顺序由强到弱
d.卤素单质与氢气化合按F2、Cl2、BR2、I2的顺序由难变易
e.最外层电子数按F、Cl、Br、I的顺序由少到多
(4)碘单质及其化合物具有重要应用.下列说法正确的是
a.
129 53 |
127 53 |
b.加碘食盐能使淀粉溶液变蓝
c.从海带食盐提取I2的过程只发生化学变化
d.提纯含沙的粗碘可用升华法.
考点:氯、溴、碘及其化合物的综合应用,位置结构性质的相互关系应用,卤素原子结构及其性质的比较
专题:元素周期律与元素周期表专题,卤族元素
分析:(1)HCl分子中共用一对电子,同一元素组成的双原子分子为非极性分子,不同种元素组成的分子为极性分子,氯气为非极性分子;
(2)根据同周期和同主族元素原子的半径变化规律,元素金属性的变化规律进行解答;
(3)第ⅥA族元素中,随着原子序数的增大得电子能力逐渐减弱、氢化物的酸性逐渐增强、单质的沸点逐渐增大、单质的氧化性逐渐减弱、氢化物的还原性逐渐增强、单质与氢气化合逐渐困难、氢化物的沸点逐渐增大(HF除外)、氢化物的稳定性逐渐减弱,据此解答;
(4)利用所学元素化合物的知识、原子结构以及元素性质的递变规律能够顺利解决此题.
(2)根据同周期和同主族元素原子的半径变化规律,元素金属性的变化规律进行解答;
(3)第ⅥA族元素中,随着原子序数的增大得电子能力逐渐减弱、氢化物的酸性逐渐增强、单质的沸点逐渐增大、单质的氧化性逐渐减弱、氢化物的还原性逐渐增强、单质与氢气化合逐渐困难、氢化物的沸点逐渐增大(HF除外)、氢化物的稳定性逐渐减弱,据此解答;
(4)利用所学元素化合物的知识、原子结构以及元素性质的递变规律能够顺利解决此题.
解答:
解:(1)反应②中形成的化合物是氯化氢,氯化氢为共价化合物,一个氢原子核外为1个电子,1个氯原子核外最外层有7个电子,HCl分子中共用一对电子,所以电子式为 ;反应③为氢原子和氯气反应,所以破坏的是氯气分子中的氯氯键,同一元素组成的双原子分子为非极性分子,所以破坏的是非极性共价键,
;反应③为氢原子和氯气反应,所以破坏的是氯气分子中的氯氯键,同一元素组成的双原子分子为非极性分子,所以破坏的是非极性共价键,
故答案为: ;非极性;
;非极性;
(2)短周期主族元素中与氯元素相邻的有F和S,根据同周期和同主族元素原子的半径变化规律同一周期,从左到右,原子序数增大,半径在逐渐减小,所以原子半径S>Cl,同一主族,从上往下,半径在逐渐增大,所以原子半径Cl>F,综上可知,三者的原子半径从大到小的顺序是S>Cl>F;与氯同周期,金属性最强的元素位于该周期的最左侧,为Na元素,钠为第三周期,第IA,
故答案为:S>Cl>F; 三;IA;
(3)a.同一主族元素单质的沸点随着原子序数的递增呈增大趋势,所以卤素单质的熔沸点按F2、Cl2、Br2、I2的顺序由低到高,故a正确;
b.电子层越多,原子半径越大,则原子半径按F、Cl、Br、I的顺序从小到大,故b错误;
c.非金属性越强,氢化物的稳定性越强,则卤素单质的稳定性按HF、HCl、HBr、HI的顺序由强到弱,故c正确;
d.非金属性越强,与氢气结合生成氢化物越容易,则卤素单质与氢气化合按F2、Cl2、Br2、I2的顺序由易变难,故d错误;
e.原子序数越大,则核外电子总数越多,最外层电子数按F、Cl、Br、I的顺序由少到多,故e正确;
故答案为:bd;
(4)a.两种核素质子数相同,中子数不同,互为同位素,故a正确;
b.加碘食盐加的是碘酸钾,而不是单质碘,碘单质使淀粉溶液变蓝,故b错误;
c.海带中提取I2,涉及到H2O2+2H++2I-═I2+2H2O的化学反应,但化学变化中一般都伴随着物理变化,故c错误;
d.碘单质能够升华,所以提纯含沙的粗碘可用升华法,故d正确;
故答案为:ad.
 ;反应③为氢原子和氯气反应,所以破坏的是氯气分子中的氯氯键,同一元素组成的双原子分子为非极性分子,所以破坏的是非极性共价键,
;反应③为氢原子和氯气反应,所以破坏的是氯气分子中的氯氯键,同一元素组成的双原子分子为非极性分子,所以破坏的是非极性共价键,故答案为:
 ;非极性;
;非极性;(2)短周期主族元素中与氯元素相邻的有F和S,根据同周期和同主族元素原子的半径变化规律同一周期,从左到右,原子序数增大,半径在逐渐减小,所以原子半径S>Cl,同一主族,从上往下,半径在逐渐增大,所以原子半径Cl>F,综上可知,三者的原子半径从大到小的顺序是S>Cl>F;与氯同周期,金属性最强的元素位于该周期的最左侧,为Na元素,钠为第三周期,第IA,
故答案为:S>Cl>F; 三;IA;
(3)a.同一主族元素单质的沸点随着原子序数的递增呈增大趋势,所以卤素单质的熔沸点按F2、Cl2、Br2、I2的顺序由低到高,故a正确;
b.电子层越多,原子半径越大,则原子半径按F、Cl、Br、I的顺序从小到大,故b错误;
c.非金属性越强,氢化物的稳定性越强,则卤素单质的稳定性按HF、HCl、HBr、HI的顺序由强到弱,故c正确;
d.非金属性越强,与氢气结合生成氢化物越容易,则卤素单质与氢气化合按F2、Cl2、Br2、I2的顺序由易变难,故d错误;
e.原子序数越大,则核外电子总数越多,最外层电子数按F、Cl、Br、I的顺序由少到多,故e正确;
故答案为:bd;
(4)a.两种核素质子数相同,中子数不同,互为同位素,故a正确;
b.加碘食盐加的是碘酸钾,而不是单质碘,碘单质使淀粉溶液变蓝,故b错误;
c.海带中提取I2,涉及到H2O2+2H++2I-═I2+2H2O的化学反应,但化学变化中一般都伴随着物理变化,故c错误;
d.碘单质能够升华,所以提纯含沙的粗碘可用升华法,故d正确;
故答案为:ad.
点评:本题考查了原子结构与元素周期律知识的综合应用,题目难度中等,试题知识点较多、综合性较强,注意掌握元素周期律内容,明确常见化学用语的概念及表示方法,试题有利于培养学生灵活应用所学知识解决实际问题的能力.

练习册系列答案
相关题目
重水D2O的离子积为1.6×10-15,可以用pH一样的定义来规定pD=-lgc(D+),以下关于pD的叙述正确的是( )
| A、中性溶液中pD=7 |
| B、在1LD2O的溶液中溶解0.01mol NaOD(设溶液的体积为1L),其中pD=12 |
| C、在1L D2O中溶解 0.01mol DCl (设溶液的体积为1L),其中pD=2 |
| D、在100 mL 0.25mol/L的DCl重水溶液中加入100 mL 0.2 mol/L的 NaOD的重水溶液,其中pD=1 |
由两种气态烃组成的混和烃的总物质的量与该混和烃充分燃烧后所得气体产物(二氧化碳和水蒸气)的物质的量的变化关系如图,以下对混和烃组成的判断中正确的是( )

| A、一定有乙烯 |
| B、一定有甲烷 |
| C、一定有丙烷 |
| D、一定有乙烷 |
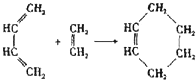 ( 也可表示为:
( 也可表示为: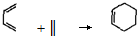 )
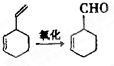
)
 X、Y、Z、W为按原子序数由小到大排列的四种短周期的元素.其申Y、W位 于同一主族,Z、W位于同一周期;Y的最外层电子数是K层电子数的3倍;Z是同一周期中金属性最强的元素,X的最外层电子数与Z相同,但X为非金属元素.请回答下列司题:
X、Y、Z、W为按原子序数由小到大排列的四种短周期的元素.其申Y、W位 于同一主族,Z、W位于同一周期;Y的最外层电子数是K层电子数的3倍;Z是同一周期中金属性最强的元素,X的最外层电子数与Z相同,但X为非金属元素.请回答下列司题: