题目内容
反应物的总能量大于生成物的总能量时,发生的反应为 热反应,中和反应都是 热反应,煅烧石灰石是 热反应.
考点:吸热反应和放热反应,中和热
专题:化学反应中的能量变化
分析:反应物的总能量大于生成物的总能量时,发生的反应为放热反应;
常见的放热反应有:所有的物质燃烧、所有金属与酸反应、金属与水反应,所有中和反应;绝大多数化合反应和铝热反应;
常见的吸热反应有:绝大数分解反应,个别的化合反应(如C和CO2),少数分解置换以及某些复分解(如铵盐和强碱),C或氢气做还原剂时的反应.
常见的放热反应有:所有的物质燃烧、所有金属与酸反应、金属与水反应,所有中和反应;绝大多数化合反应和铝热反应;
常见的吸热反应有:绝大数分解反应,个别的化合反应(如C和CO2),少数分解置换以及某些复分解(如铵盐和强碱),C或氢气做还原剂时的反应.
解答:
解:反应物的总能量大于生成物的总能量时,发生的反应为放热反应;
中和反应是放热反应;
煅烧石灰石是分解反应是吸热反应,故答案为:放;放;吸.
中和反应是放热反应;
煅烧石灰石是分解反应是吸热反应,故答案为:放;放;吸.
点评:本题考查放热反应,难度不大,抓住中学化学中常见的吸热或放热的反应是解题的关键,对于特殊过程中的热量变化的要熟练记忆来解答此类习题.

练习册系列答案
 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案
相关题目
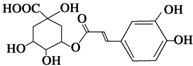 预防和治疗甲型H1N1流感的中草药中都含有金银花.绿原酸是金银花的活性成分之一,具有广泛的抗菌及抗病毒作用.有关绿原酸的说法错误的是( )
预防和治疗甲型H1N1流感的中草药中都含有金银花.绿原酸是金银花的活性成分之一,具有广泛的抗菌及抗病毒作用.有关绿原酸的说法错误的是( )| A、绿原酸的分子式为C16H18O9 |
| B、1 mol绿原酸最多可与5 mol H2发生反应 |
| C、绿原酸中含氧官能团有羧基、羟基和酯基 |
| D、绿原酸酸性条件下水解后所得两产物碳原子数之差为2 |
国家质检部门检出人们端午节包粽子的“返青粽叶”多以硫酸铜为添加剂,长期食用有害健康,请问硫酸铜是一种( )
| A、氧化物 | B、盐 | C、碱 | D、酸 |
工业废水中常含有一定量的Cr2O72-,会对人类及生态系统产生很大损害,电解法是一种行之有效的除去铬的方法之一.该法用Fe作电极电解含Cr2O72-的酸性废水,最终将铬转化为Cr(OH)3沉淀,达到净化目的.下列有关说法不正确的是( )
| A、电解时选用Fe作阳极,石墨棒作阴极 |
| B、阴极附近的沉淀只有Cr(OH)3 |
| C、阳极附近溶液中,发生反应的离子方程式是Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O |
| D、消耗1mol Cr2O72-,将有336g Fe消耗,因此要定期更换铁电极 |
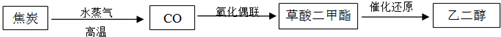
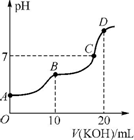
 已知化学反应N2+3H2=2NH3的能量变化如图所示,
已知化学反应N2+3H2=2NH3的能量变化如图所示,