题目内容
9.某校化学兴趣小组用如图所示过程除去AlCl3溶液中含有的Mg2+、K+杂质离子并尽可能减少AlCl3的损失.
下列说法正确的是( )
| A. | NaOH溶液可以用氨水来代替 | |
| B. | 溶液a中含有Al3+、K+、Cl-、Na+、OH- | |
| C. | 溶液b中只含有NaCl | |
| D. | 向溶液a中滴加盐酸需控制溶液的pH |
分析 由实验流程可知,加足量的NaOH生成氢氧化镁沉淀,溶液a中含AlO2-、K+、Cl-、Na+、OH-,然后加盐酸,沉淀a为氢氧化铝,溶液b中含KCl、NaCl,以此来解答.
解答 解:A.用氨水,则Mg2+、Al3+均转化为沉淀,不能分离,则不能用氨水代替NaOH,故A错误;
B.Al3+与过量NaOH反应,溶液a中含AlO2-、K+、Cl-、Na+、OH-,故B错误;
C.K+、Cl-、Na+在整个过程中不参加反应,则溶液b中含KCl、NaCl,故C错误;
D.因氢氧化铝能溶于盐酸,则向溶液a中滴加盐酸需控制溶液的pH,故D正确;
故选D.
点评 本题考查混合物分离、提纯实验方案的设计,为高频考点,把握实验流程中发生的反应为解答的关键,侧重分析与实验能力的考查,注意氢氧化铝的两性,题目难度不大.

练习册系列答案
相关题目
20.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 1mol固体氯化氨中存在离子数小于2NA | |
| B. | 标准状况下,22.4L己烷中共价键的数目为19NA | |
| C. | 标况下的NO2气体22.4L,其中含有的氮原子数为NA | |
| D. | 常温常压下,3.0g含甲醛的冰醋酸中含有的原子总数为0.4NA |
17.研究人员最近发现了一种“水”电池,这种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反应可表示为:5MnO2+2Ag+2NaCl═Na2Mn5O10+2AgCl,下列“水”电池在海水中放电时的有关说法不正确的是( )
| A. | 负极反应式:Ag+Cl--e-═AgCl | |
| B. | AgCl是氧化产物 | |
| C. | 每生成1 mol Na2Mn5O10转移2 mol电子 | |
| D. | Na+不断向“水”电池的负极移动 |
1.NaH与水反应的化学方程式为NaH+H2O═NaOH+H2↑,对该反应叙述中正确的是( )
| A. | 该反应属于置换反应 | |
| B. | NaH中的H为+1价 | |
| C. | 氧化剂是H2O | |
| D. | 每摩尔NaH参加反应时电子转移数为1e- |
 到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源.
到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源.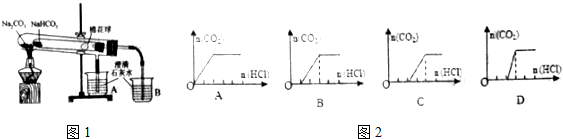
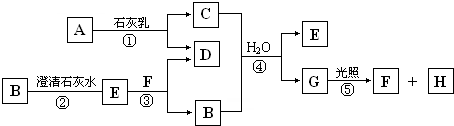
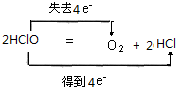 .
.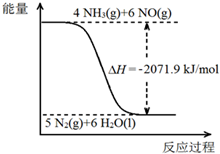 尿素[CO(NH2)2]是一种高效化肥,也是一种化工原料.以尿素为原料在一定条件下发生反应:CO(NH2)2 (s)+H2O(l)?2NH3(g)+CO2(g)△H=+133.6kJ/mol.尿素在一定条件下可将氮的氧化物还原为氮气.
尿素[CO(NH2)2]是一种高效化肥,也是一种化工原料.以尿素为原料在一定条件下发生反应:CO(NH2)2 (s)+H2O(l)?2NH3(g)+CO2(g)△H=+133.6kJ/mol.尿素在一定条件下可将氮的氧化物还原为氮气.