题目内容
2.下列说法正确的是( )| A. | 用丁达尔效应鉴别氢氧化铁胶体和氯化铁溶液 | |
| B. | 因为SO2有漂白性,所以它可使紫色石蕊溶液褪色 | |
| C. | 氯化钠溶液在电流作用下电离成Na+离子和Cl-离子 | |
| D. | 等质量的碳酸钠和碳酸氢钠与足量盐酸反应时,碳酸钠产生的CO2多 |
分析 A.胶体的特征性质为丁达尔现象,溶液无此现象;
B.二氧化硫的漂白性具有选择性,通入石蕊试液指表现亚硫酸的酸性;
C.电解质电离是水分子作用下电离成自由移动的离子;
D.等质量的碳酸钠和碳酸氢钠,物质的量碳酸氢钠大于碳酸钠,结合碳元素守恒分析判断.
解答 解:A.用丁达尔效应可以鉴别氢氧化铁胶体和氯化铁溶液,当光线通过胶体会出现光亮的通路,通过溶液无此现象,故A正确;
B.二氧化硫的漂白性具有选择性,选择品红溶液褪色,通入石蕊试液指表现亚硫酸的酸性,溶液变红色,故B错误;
C.氯化钠溶液在水分子作用下电离成Na+离子和Cl-离子,不需要通电,故C错误;
D.等质量的碳酸钠和碳酸氢钠,物质的量碳酸氢钠大于碳酸钠,与足量盐酸反应时,碳酸氢钠产生的CO2多,故D错误;
故选A.
点评 本题考查了胶体性质,二氧化硫、碳酸氢钠和碳酸钠的性质,主要是二氧化硫漂白性的理解应用,题目难度中等.

练习册系列答案
相关题目
12.下列药品可用带玻璃塞的试剂瓶存放的是( )
| A. | NaOH溶液 | B. | Na2CO3溶液 | C. | 盐酸 | D. | 水玻璃 |
13.下列说法正确的是( )
| A. | 金属钠应保存在四氯化碳里以隔绝空气 | |
| B. | 高温下铁能与水蒸气反应生成氢气和三氧化二铁 | |
| C. | 漂白粉应隔绝空气密封保存,并放置在干燥避光的环境中 | |
| D. | 铝较活泼,所以铝制品在空气中不能稳定存在 |
10.用下列实验装置进行相应实验,装置正确且能达到实验目的是( )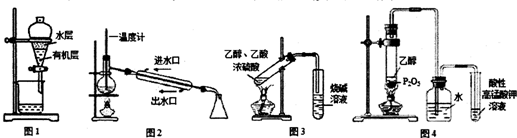

| A. | 用图1所示装置分离用苯萃取碘水后已分层的有机层和水层 | |
| B. | 用图2所示装置进行石油的分馏 | |
| C. | 用图3所示装置制备少量的乙酸乙酯 | |
| D. | 用图4所示装置制取乙烯并验证其易被氧化 |
17.为除去铜粉中混有的少量铝粉,下列试剂不可行的是( )
| A. | CuCl2溶液 | B. | 稀硝酸 | C. | NaOH溶液 | D. | 稀盐酸 |
7.下列实验操作或装置正确的是( )


| A. | 利用图1所示装置吸收制取少量二氧化硫产生的尾气 | |
| B. | 利用图2所示装置制取乙烯 | |
| C. | 利用图3所示装置证明H2CO3酸性强于苯酚 | |
| D. | 利用图4所示装置制备乙酸乙酯 |
14.下列物质中的主要成分不属于糖类的是( )
| A. | 棉花 | B. | 木材 | C. | 小麦 | D. | 羊毛 |
11.下面各容器中盛有海水,铁在其中被腐蚀时由快到慢的顺序是( )
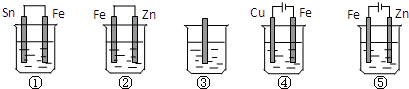

| A. | ①>②>③>④>⑤ | B. | ⑤>①>③>②>④ | C. | ⑤>①>②>③>④ | D. | ⑤>②>①>③>④ |
15.下列实验方案鉴別Na2CO3和NaHCO3,粉末能达到预期目的是( )
| A. | 分别加等体枳、等浓度的稀盐酸,比较生成气体的快慢 | |
| B. | 分别加等体积适量的水,比较固体溶解量的多少 | |
| C. | 分别将两种粉末配成溶液,然后加入澄清的石灰水,比较是否有沉淀生成 | |
| D. | 分別将两种粉末加热,并将产生的气体通入澄清的石灰水,比较澄清石灰水是否变涿浊 |