题目内容
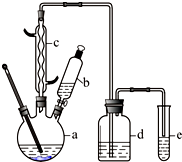 溴苯是一种化工原料,某兴趣小组用如下装置制备溴苯并证明苯和液溴发生的是取代反应,而不是加成反应.有关数据如下:
溴苯是一种化工原料,某兴趣小组用如下装置制备溴苯并证明苯和液溴发生的是取代反应,而不是加成反应.有关数据如下:| 苯 | 溴 | 溴苯 | |
| 密度/g?cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |
(1)仪器c的名称为
(2)将b中液溴缓慢滴入a瓶的无水苯及铁的混合体系中,充分反应即可得到溴苯,通过下列步骤分离提纯:
①向a中加入10mL水,然后
②产品依次用10mL水、10%的NaOH溶液、10mL水洗涤.此过程需要分液操作,分液时溴苯应从
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤.
(3)经过上述分离操作后,粗溴苯中还含有的主要杂质为
(4)装置d中所装的试剂为
(5)能证明苯和液溴发生的是取代反应,而不是加成反应,进行的操作及现象是
考点:制备实验方案的设计
专题:实验设计题
分析:(1)由仪器的形状可知仪器的名称;
(2)将b中液溴缓慢滴入a瓶的无水苯及铁的混合体系中,充分反应即可得到溴苯,通过下列步骤分离提纯:
①根据铁屑不溶于水判断;
②根据分液操作时应选的仪器为分液漏斗,并且分液时应遵循上层液体从上层倒出,下层液体从下口放出来分析;
(3)反应后得到的溴苯中溶有少量苯杂质,依据它和溴苯的性质不同除杂;
(4)根据苯与溴发生的取代反应生成溴化氢,但由于溴具有挥发性,所以制得的溴化氢中含有溴蒸气,利用溴单质易溶于有机溶剂,所以应选用CCl4除去HBr中的Br2,据此解答;
(5)根据苯和溴发生取代反应生成溴化氢,设计实验证明反应后的溶液中含有溴离子即可;
(2)将b中液溴缓慢滴入a瓶的无水苯及铁的混合体系中,充分反应即可得到溴苯,通过下列步骤分离提纯:
①根据铁屑不溶于水判断;
②根据分液操作时应选的仪器为分液漏斗,并且分液时应遵循上层液体从上层倒出,下层液体从下口放出来分析;
(3)反应后得到的溴苯中溶有少量苯杂质,依据它和溴苯的性质不同除杂;
(4)根据苯与溴发生的取代反应生成溴化氢,但由于溴具有挥发性,所以制得的溴化氢中含有溴蒸气,利用溴单质易溶于有机溶剂,所以应选用CCl4除去HBr中的Br2,据此解答;
(5)根据苯和溴发生取代反应生成溴化氢,设计实验证明反应后的溶液中含有溴离子即可;
解答:
解:(1)由仪器的形状可知c为冷凝管故答案为:冷凝管;
(2)①由于铁屑不溶于水溶液,所以用过滤的方法除去未反应的铁屑,故答案为:过滤;
②由于分液操作应在分液漏斗中进行,又溴苯的密度比水大,所以应在下层,故答案为:分液漏斗;下口;
(3)反应后得到的溴苯中溶有少量未反应的苯,苯和溴苯互溶,但苯的沸点低,所以采用蒸馏的方法进行分离,溴苯留在母液中,
故答案为:苯;蒸馏;
(4)由于溴具有挥发性,制得的溴化氢中含有溴蒸气,利用溴单质易溶于有机溶剂,所以应选用CCl4除去HBr中的Br2,故答案为:CCl4; 除去HBr气体中的Br2;
(5)苯和溴发生取代反应生成溴化氢,故利用稀硝酸和硝酸银检验出反应后有溴离子则可证明,所以操作及现象为取e中溶液注入试管中,加硝酸酸化的AgNO3溶液,若产生浅黄色沉淀,则苯和液溴发生的是取代反应;故答案为:取e中溶液注入试管中,加硝酸酸化的AgNO3溶液,若产生浅黄色沉淀,则苯和液溴发生的是取代反应;
(2)①由于铁屑不溶于水溶液,所以用过滤的方法除去未反应的铁屑,故答案为:过滤;
②由于分液操作应在分液漏斗中进行,又溴苯的密度比水大,所以应在下层,故答案为:分液漏斗;下口;
(3)反应后得到的溴苯中溶有少量未反应的苯,苯和溴苯互溶,但苯的沸点低,所以采用蒸馏的方法进行分离,溴苯留在母液中,
故答案为:苯;蒸馏;
(4)由于溴具有挥发性,制得的溴化氢中含有溴蒸气,利用溴单质易溶于有机溶剂,所以应选用CCl4除去HBr中的Br2,故答案为:CCl4; 除去HBr气体中的Br2;
(5)苯和溴发生取代反应生成溴化氢,故利用稀硝酸和硝酸银检验出反应后有溴离子则可证明,所以操作及现象为取e中溶液注入试管中,加硝酸酸化的AgNO3溶液,若产生浅黄色沉淀,则苯和液溴发生的是取代反应;故答案为:取e中溶液注入试管中,加硝酸酸化的AgNO3溶液,若产生浅黄色沉淀,则苯和液溴发生的是取代反应;
点评:本题主要考查了溴苯的制取实验、物质的分离提纯等,清楚制备的原理是解答的关键,题目难度中等.

练习册系列答案
相关题目
反应SiCl4+2H2
Si(纯)+4HCl可用于工业制取纯硅.该反应属于( )
| ||
| A、化合反应 | B、复分解反应 |
| C、置换反应 | D、分解反应 |
在同温同压下,10L气体A2跟30L气体B2恰好完全化合生成20L气体C,则气体C的化学式(用A、B表示)为( )
| A、AB |
| B、A2B |
| C、AB2 |
| D、AB3 |
下列化学用语表示不正确的是( )
| A、氮化镁的化学式:MgN | ||||
B、中子数为18的氯原子:
| ||||
| C、Ca(OH)2的电离方程式:Ca(OH)2═Ca2++2OH- | ||||
D、铁在氯气中燃烧:2Fe+3Cl2
|
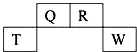 如图为元素周期表中短周期的一部分,四种元素中只有一种是金属,下列说法不正确的是( )
如图为元素周期表中短周期的一部分,四种元素中只有一种是金属,下列说法不正确的是( )| A、气态氢化物稳定性:R>Q |
| B、Q与W可形成直线型分子QW2 |
| C、同主族气态氢化物中R的氢化物最稳定,因其分子间存在氢键 |
| D、原子半径:T>W,简单离子半径:T<W |
已知298K时,合成氨反应N2(g)+3H2(g)═2NH3(g)△H=-92.0kJ?mol-1,将此温度下的1mol N2和3mol H2放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量为(假定测量过程中没有能量损失)( )
| A、一定大于92.0 kJ |
| B、无法确定 |
| C、一定小于92.0 kJ/mol |
| D、一定小于92.0 kJ |
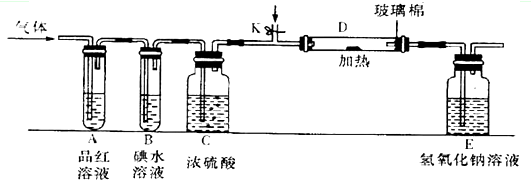
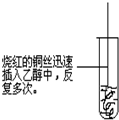 乙醇的催化氧化,看右图答出实验现象.
乙醇的催化氧化,看右图答出实验现象.