题目内容
 现有A、B、C、D、E、F六种物质,其中A、B、C是由短周期元素组成的常见单质,D分子含有10个电子,F是一种不含金属元素的盐.一定条件下转化关系如图:
现有A、B、C、D、E、F六种物质,其中A、B、C是由短周期元素组成的常见单质,D分子含有10个电子,F是一种不含金属元素的盐.一定条件下转化关系如图:请回答:
(1)组成A的元素在周期表中的位置是
(2)下列关于D的说法正确的是
a.有还原性 b.其水溶液能使酚酞溶液变红色
c.极易溶于水 d.其水溶液能使品红溶液褪色
(3)F与消石灰共热反应,可用于制取D气体,反应的化学方程式是
(4)一定条件下E的浓溶液和二氧化锰加热反应能生成C,当生成标准状况下1.12L C时,转移电子的物质的量为
考点:无机物的推断
专题:推断题
分析:F是一种不含金属元素的盐,则F为铵盐,A、B、C是由短周期元素组成的常见单质,D分子含有10个电子,结合转化关系可知,B为H2,A为N2,D为NH3,C为Cl2,E为HCl,则F为NH4Cl,以此来解答.
解答:
解:F是一种不含金属元素的盐,则F为铵盐,A、B、C是由短周期元素组成的常见单质,D分子含有10个电子,结合转化关系可知,B为H2,A为N2,D为NH3,C为Cl2,E为HCl,则F为NH4Cl,
(1)组成A的元素为N,位于第二周期第VA族,故答案为:第二周期第VA族;
(2)a.氨气中N元素的化合价为-3价,为最低价,有还原性,故正确;
b.其水溶液中一水合氨电离出氢氧根离子,显碱性,能使酚酞溶液变红色,故正确;
c.氨气与水形成氢键,极易溶于水,故正确;
d.其水溶液不具有漂白性,则不能使品红溶液褪色,故错误;
故答案为:abc;
(3)F与消石灰共热反应,可用于制取D气体,反应的化学方程式是2NH4Cl+Ca(OH)2
CaCl2+2H2O+2NH3↑,
故答案为:;
(4)由Cl元素的化合价变化可知,生成标准状况下1.12L C时,转移电子为
×2×[0-(-1)]=0.1mol,故答案为:0.1.
(1)组成A的元素为N,位于第二周期第VA族,故答案为:第二周期第VA族;
(2)a.氨气中N元素的化合价为-3价,为最低价,有还原性,故正确;
b.其水溶液中一水合氨电离出氢氧根离子,显碱性,能使酚酞溶液变红色,故正确;
c.氨气与水形成氢键,极易溶于水,故正确;
d.其水溶液不具有漂白性,则不能使品红溶液褪色,故错误;
故答案为:abc;
(3)F与消石灰共热反应,可用于制取D气体,反应的化学方程式是2NH4Cl+Ca(OH)2
| ||
故答案为:;
(4)由Cl元素的化合价变化可知,生成标准状况下1.12L C时,转移电子为
| 1.12L |
| 22.4L/mol |
点评:本题考查无机物的推断,为高频考点,把握F为铵盐及D为10电子微粒等推断物质为解答的关键,侧重非金属及其化合物性质、相互转化的考查,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列物质按只含离子键、只含共价键、既含离子键又含共价键的顺序排列的是( )
| A、氯气 二氧化碳 氢氧化钠 |
| B、氯化钠 过氧化钠 氯化铵 |
| C、氯化钠 过氧化氢 氯化铵 |
| D、氯化钠 氦气 氢氧化钠 |
下列离子方程式书写正确的是( )
| A、铜和硝酸银反应:Cu+Ag+═Cu2++Ag | ||||
| B、NaHCO3溶液与稀H2SO4反应:CO32-+2H+═H2O+CO2↑ | ||||
| C、稀HNO3中加入少量铁粉:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O | ||||
D、NH4Cl和NaOH的两浓溶液混合加热:NH4++OH-
|
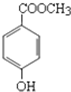 尼泊金酯是一种高效食品防腐剂,其结构简式为:
尼泊金酯是一种高效食品防腐剂,其结构简式为: