题目内容
9.常温下pH为2的盐酸,下列叙述正确的是( )| A. | 将10 mL该溶液稀释至100 mL后,pH=4 | |
| B. | 向该溶液中加入等体积pH为12的氨水恰好完全中和 | |
| C. | 该溶液中盐酸电离出的c(H+)与水电离出的c(H+)之比为1010:1 | |
| D. | 该溶液中由水电离出的c(H+)水×c(OH-)水=1×10-14 |
分析 A、盐酸溶液中氯化氢完全电离,溶液稀释10倍,溶液pH增大一个单位;
B、一水合氨是弱电解质存在电离平衡;
C、常温下pH为2的盐酸溶液中,水电离出的氢氧根离子浓度和氢离子浓度相同为10-12mol/L;
D、常温下pH为2的盐酸溶液中酸中氢离子浓度为10-2mol/L,水电离出的氢离子浓度为10-12mol/L.
解答 解:A、盐酸溶液中氯化氢完全电离,溶液稀释10倍,溶液pH增大一个单位,将10mL该溶液稀释至100mL后,pH等于3,故A错误;
B、一水合氨是弱电解质存在电离平衡,向该溶液中加入等体积pH为12的氨水,平衡状态下的氢氧根离子恰好完全中和,一水合氨又电离出氢氧根离子,一水合氨过量,故B错误;
C、pH为2的盐酸溶液中酸中氢离子浓度为10-2mol/L,水电离出的氢离子浓度为10-12mol/L,溶液中盐酸电离的c(H+)与水电离出的c(H+)之比为1010:1,故C正确;
D、常温下pH为2的盐酸溶液中,水电离出的氢氧根离子浓度和氢离子浓度相同为10-12mol/L,由水电离出的c(H+),c(水)×c(OH-)(水)=1×10-24,故D错误;
故选C.
点评 本题考查了水的电离分析,弱电解质电离平衡的理解应用,掌握溶液中离子积常数的计算方法和含义是解题关键,题目难度中等.

练习册系列答案
相关题目
19.酚酞的结构如图,则下列说法中正确的是( )


| A. | 分子式是C20H12O4 | B. | 能与NaOH稀溶液反应,溶液显红色 | ||
| C. | 能与溴水反应,溶液显红色 | D. | 与羧酸发生酯化反应 |
20.室温时,将浓度和体积分别为c1,V1的NaOH溶液和c2、V2的CH3COOH溶液相混合,下列关于该混合溶液的叙述错误的是( )
| A. | 当pH=7时,若V1=V2,则一定是c2>c1 | |
| B. | 在任何情况下都满足c(Na+)+c(H+)=c(CH3COO-)+c(OH-) | |
| C. | 若pH>7,则一定是c1V1>c2V2 | |
| D. | 若V1=V2,c1=c2,则c(CH3COO-)+c(CH3COOH)=c(Na+) |
17.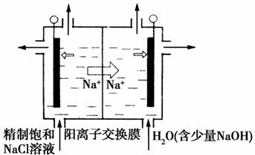 二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.目前已开发出用电解法制取ClO2的新工艺.
二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.目前已开发出用电解法制取ClO2的新工艺.
(1)①如图装置用石墨作电极,在一定条件下电解饱和食盐水制取ClO2.写出阳极产生ClO2的电极反应式:Cl--5e-+2H2O=ClO2↑+4H+.
②电解一段时间,当阴极产生的气体体积为112mL(标准状况)时,停止电解.通过阳离子交换膜的阳离子的物质的量为0.01mol.
(2)为提高甲醇燃料的利用率,科学家发明了一种燃料电池,电池的一个电极通入空气,另一个电极通入甲醇气体,电解质是掺入了Y2O3的ZrO2晶体,在高温下它能传导O2-离子.电池工作时正极反应为O2+4e-=2O2-.
(3)若以该电池为电源,用石墨做电极电解100mL含有如下离子的溶液.
电解一段时间后,当两极收集到相同体积(相同条件)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象)阳极上收集到氧气的物质的量为0.1mol.
 二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.目前已开发出用电解法制取ClO2的新工艺.
二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.目前已开发出用电解法制取ClO2的新工艺.(1)①如图装置用石墨作电极,在一定条件下电解饱和食盐水制取ClO2.写出阳极产生ClO2的电极反应式:Cl--5e-+2H2O=ClO2↑+4H+.
②电解一段时间,当阴极产生的气体体积为112mL(标准状况)时,停止电解.通过阳离子交换膜的阳离子的物质的量为0.01mol.
(2)为提高甲醇燃料的利用率,科学家发明了一种燃料电池,电池的一个电极通入空气,另一个电极通入甲醇气体,电解质是掺入了Y2O3的ZrO2晶体,在高温下它能传导O2-离子.电池工作时正极反应为O2+4e-=2O2-.
(3)若以该电池为电源,用石墨做电极电解100mL含有如下离子的溶液.
| 离子 | Cu2+ | H+ | Cl- | SO42- |
| c/mol•L-1 | 1 | 4 | 4 | 1 |
4.常温下,用0.10mol•L-1NaOH溶液分别滴定20.00mL浓度均为0.10mol•L-1的CH3COOH溶液和HCN溶液,滴定曲线如图所示.下列说法不正确的是( )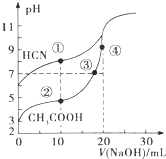

| A. | 点③溶液中,c(OH-)=c(H+)+c(CH3COOH) | |
| B. | 点①溶液的c(CN-)<点②溶液的c(CH3COO-) | |
| C. | 点④溶液中,c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | |
| D. | 在点②和③之间(不包括端点)存在离子浓度大小关系:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
18.NA为阿伏伽徳罗常数的值,下列说法正确的是( )
| A. | 1L 1mol/L的稀硝酸中,氧原子数为3NA | |
| B. | 常温常压下的67.2L氯气与54g铝充分反应,转移电子数为6NA | |
| C. | 过氧化钠与水反应时,生成0.1mol氧气转移的电数为0.2NA | |
| D. | 标准状况下,80gSO3,中含3NA心个氧原子,体积约为22.4L |
19.下列实验装置不能达到实验目的是( )
| A. | 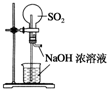 用SO2做喷泉实验 | B. |  干燥氯气 | ||
| C. | 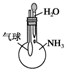 验证NH3易溶于水 | D. | 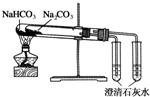 比较Na2CO3与NaHCO3的稳定性 |