题目内容
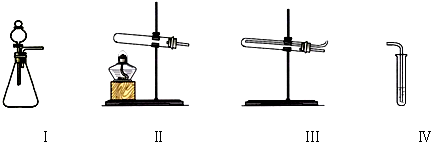
据媒体报道,2009年2月12日我外交部就法国佳士得公司拍卖我圆明园兔首和鼠首两件文物(如图1),发表严正声明:中国对其拥有不可置疑的所有权.这两件文物均为青铜器,其表面呈绿色,查阅资料得知,这是铜
器长期暴露在空气中生成了铜绿[Cu2(OH)2CO3],铜绿不稳定,受热易分解.
(1)根据铜绿的组成,可以推测铜绿的形成是铜与 (填化学式)作用的结果.
(2)除题目中已有的说明,请再写出铜绿的一种物理性质和一种化学性质:物理性质: ,化学性质: .
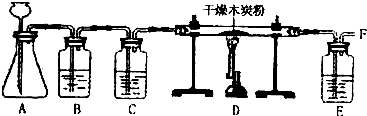
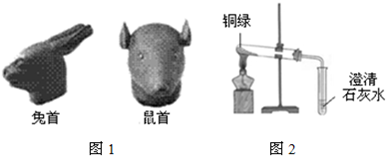
(3)为了探究铜绿的性质,小王同学从其它铜器上刮下适量铜绿,放入图2装置中,加热后,可以观
察到的现象有 .
(4)小李同学偶然发现一腐蚀严重的金属片表面呈绿色,但从其硬度和重量估计不是铜片,小李查阅资料后猜测其为一种铝合金(主要含铝、铜以及少量镁).请你设计一个实验验证该金属片中含铝和铜,写出简要的操作步骤、预期现象及结论.(仪器和试剂不限)
器长期暴露在空气中生成了铜绿[Cu2(OH)2CO3],铜绿不稳定,受热易分解.

(1)根据铜绿的组成,可以推测铜绿的形成是铜与
(2)除题目中已有的说明,请再写出铜绿的一种物理性质和一种化学性质:物理性质:
(3)为了探究铜绿的性质,小王同学从其它铜器上刮下适量铜绿,放入图2装置中,加热后,可以观
察到的现象有
(4)小李同学偶然发现一腐蚀严重的金属片表面呈绿色,但从其硬度和重量估计不是铜片,小李查阅资料后猜测其为一种铝合金(主要含铝、铜以及少量镁).请你设计一个实验验证该金属片中含铝和铜,写出简要的操作步骤、预期现象及结论.(仪器和试剂不限)
| 操作步骤 | 预期现象及结论 |
考点:性质实验方案的设计
专题:实验设计题
分析:(1)铜器长期暴露在空气中生成了铜绿[Cu2(OH)2CO3],碳元素来自空气中二氧化碳,氢元素来自空气中水蒸汽,氧元素来自二氧化碳和氧气;
(2)铜绿能在空气中存在,故应难溶于水,铜绿属于碱式碳酸盐,应能和酸反应;
(3)铜绿不稳定,受热分解为氧化铜、二氧化碳和水,二氧化碳遇澄清石灰水变浑浊;
(4)铝和碱反应,铜不和碱反应,但铜可与稀硝酸反应,据此设计实验方案.
(2)铜绿能在空气中存在,故应难溶于水,铜绿属于碱式碳酸盐,应能和酸反应;
(3)铜绿不稳定,受热分解为氧化铜、二氧化碳和水,二氧化碳遇澄清石灰水变浑浊;
(4)铝和碱反应,铜不和碱反应,但铜可与稀硝酸反应,据此设计实验方案.
解答:
解:(1)铜器长期暴露在空气中生成了铜绿[Cu2(OH)2CO3],碳元素来自空气中二氧化碳,氢元素来自空气中水蒸汽,氧元素来自二氧化碳和氧气;
故答案为:O2、H2O、CO2;
(2)铜绿能在空气中存在,故应难溶于水,铜绿属于碱式碳酸盐,应能和酸反应;
故答案为:难溶于水;可溶于酸;
(3)铜绿不稳定,受热分解为氧化铜、二氧化碳和水,二氧化碳遇澄清石灰水变浑浊,故看到的现象为:
固体由绿色变成黑色,大试管口有水珠凝结,导管口有气泡冒出,澄清石灰水变浑浊;
故答案为:固体由绿色变成黑色,大试管口有水珠凝结,导管口有气泡冒出,澄清石灰水变浑浊;
(4)铝和碱反应,把金属片放在氢氧化钠溶液中应有气泡产生,过滤后,向滤液中加入盐酸应出现先沉淀后溶解的现象,反应方程式为:2Al+2H2O+2NaOH=2NaAlO2+3H2↑,NaAlO2+HCl+H2O═Al(OH)3↓+NaCl、Al(OH)3+3HCl=AlCl3+3H2O;过滤后滤渣为铜,加入稀硝酸,发生反应:3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O;
故看到现象为:固体全部溶解,有无色刺激性气体产生并很快变成红棕色,溶液显蓝色,加NaOH溶液后有蓝色沉淀产生,证明含铜;
故答案为:
(另一思路:先酸溶,过滤,滤渣验铜,滤液加入过量碱液,再过滤后加酸验铝.)
故答案为:O2、H2O、CO2;
(2)铜绿能在空气中存在,故应难溶于水,铜绿属于碱式碳酸盐,应能和酸反应;
故答案为:难溶于水;可溶于酸;
(3)铜绿不稳定,受热分解为氧化铜、二氧化碳和水,二氧化碳遇澄清石灰水变浑浊,故看到的现象为:
固体由绿色变成黑色,大试管口有水珠凝结,导管口有气泡冒出,澄清石灰水变浑浊;
故答案为:固体由绿色变成黑色,大试管口有水珠凝结,导管口有气泡冒出,澄清石灰水变浑浊;
(4)铝和碱反应,把金属片放在氢氧化钠溶液中应有气泡产生,过滤后,向滤液中加入盐酸应出现先沉淀后溶解的现象,反应方程式为:2Al+2H2O+2NaOH=2NaAlO2+3H2↑,NaAlO2+HCl+H2O═Al(OH)3↓+NaCl、Al(OH)3+3HCl=AlCl3+3H2O;过滤后滤渣为铜,加入稀硝酸,发生反应:3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O;
故看到现象为:固体全部溶解,有无色刺激性气体产生并很快变成红棕色,溶液显蓝色,加NaOH溶液后有蓝色沉淀产生,证明含铜;
故答案为:
| 操作步骤 | 预期现象及结论 |
| 1、剪一小块金属片放入试管A中,加入足量的NaOH溶液,充分反应后过滤,得滤渣1和滤液1. | 金属片大部分溶解得到无色溶液,有气泡产生,初步证明含铝; |
| 2、取少量滤液1于试管B中,逐滴滴加盐酸至过量. | 先有白色沉淀生成后沉淀又溶解,证明含铝; |
| 3、取滤渣1于试管C中,加入足量盐酸,充分反应后过滤,洗涤,得滤渣2和滤液2. | 固体部分溶解,溶液可能呈蓝色,剩余固体为红色,初步证明含铜; |
| 4、取滤渣2于试管D中,加入稀硝酸,再滴加NaOH溶液. | 固体全部溶解,有无色刺激性气体产生并很快变成红棕色,溶液显蓝色,加NaOH溶液后有蓝色沉淀产生,证明含铜. |
点评:本题考查了铜绿成分的检验的实验方案的设计,中等难度,注意结合题给信息解答,设计铝合金的检验时要从铝既能和酸反应又能和碱反应去设计,可有不同的思路.

练习册系列答案
相关题目
用足量的MnO2和含HCl为4mol的浓盐酸充分反应(共热),在不考虑HCl挥发的情况下,得到的氯气( )
| A、等于2mol |
| B、等于1mol |
| C、小于1mol |
| D、大于2mol |
下列叙述正确的是( )
| A、将5.85g NaCl晶体溶入100mL水中,制得0.1mol/L的NaCl溶液 | ||
| B、将25g无水CuSO4溶于水制成100mL溶液,其浓度为1mol/L | ||
C、将wga% 的NaCl溶液蒸发掉
| ||
| D、将1体积1mol/L的硫酸用水稀释为5体积,稀溶液的浓度为0.2mol/L |