题目内容
取50.0 ml Na2CO3和Na2SO4的混合溶液,加入过量BaCl2溶液后得到14.51 g白色沉淀,用过量稀硝酸处理后沉淀量减少到4.66 g,并有气体放出.试计算:?
(1)原混合溶液中Na2CO3和Na2SO4的物质的量浓度.?
(2)产生的气体在标准状况下的体积.
:(1)1.0 mol·L-1 0.40 mol·L-1
(2)1.12 L
解析:
本题是关于混合物的计算题.?
Na2CO3和Na2SO4混合溶液中加入过量BaCl2溶液后,产生的白色沉淀是BaCO3和BaSO4的混合物.向沉淀中加入过量硝酸后,BaSO4不溶解,BaCO3溶解并放出CO2,剩余的4.66 g沉淀为BaSO4.
由生成的BaCO3、BaSO4的质量,可求得它们的物质的量;它们的物质的量也分别是Na2CO3和Na2SO4的物质的量,从而求得Na2CO3、Na2SO4的物质的量浓度,生成CO2的体积可由化学方程式求出.?
解:Na2CO3+BaCl2=BaCO3↓+2NaCl?
Na2SO4+BaCl2=BaSO4↓+2NaCl?
BaCO3+2HNO3=Ba(NO3)2+CO2↑+H2O?
(1)n(Na2SO4)=n(BaSO4)=![]() =0.02 mol?
=0.02 mol?
m(BaCO3)=14.51g-4.66g=9.85g?
n(Na2CO3)=n(BaCO3)=![]() =0.05 molc(Na2SO4)=
=0.05 molc(Na2SO4)=![]() =0.40 mol·L-1?
=0.40 mol·L-1?
c(Na2CO3)=![]() =1.0 mol·L-1?
=1.0 mol·L-1?
(2)n(CO2)=n(Na2CO3)=0.05 mol?
VHCO2)=0.05 mol×22.4 L·mol-1=1.12 L

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
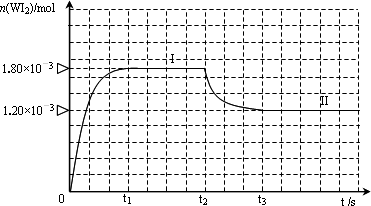
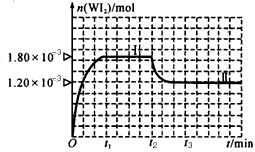
 WI2(g)。为模拟上述反应,在实验室中准确称取
WI2(g)。为模拟上述反应,在实验室中准确称取