题目内容
(13分)在周期表中,同一主族元素化学性质相似。目前也发现有些元素的化学性质和它在周期表中左上方或右下方的另一主族元素性质相似,这称为对角线规则。据此请回答:
(1)锂在空气中燃烧主要产物的电子式是 ,同时生成微量的_____ ;
(2)铍的最高价氧化物对应的水化物的化学式是_________________,它属两性化合物,证明这一结论的有关离子方程______________________ _,__________ ____;
(3)若已知反应Be2C+4H2O===2Be(OH)2+CH4↑,则Al4C3遇强碱溶液反应的离子方程式为____________________________________;
(4)科学家证实,BeCl2属共价化合物,设计一个简单实验证明,其方法是______________,用电子式表示BeCl2的形成过程:________________________________________。
(1)锂在空气中燃烧主要产物的电子式是 ,同时生成微量的_____ ;
(2)铍的最高价氧化物对应的水化物的化学式是_________________,它属两性化合物,证明这一结论的有关离子方程______________________ _,__________ ____;
(3)若已知反应Be2C+4H2O===2Be(OH)2+CH4↑,则Al4C3遇强碱溶液反应的离子方程式为____________________________________;
(4)科学家证实,BeCl2属共价化合物,设计一个简单实验证明,其方法是______________,用电子式表示BeCl2的形成过程:________________________________________。

 (12分) (1)
(12分) (1) 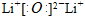 Li3N (各1分)
Li3N (各1分)(2)Be(OH)2 Be(OH)2+2H+===Be2++2H2O
Be(OH)2+2OH-===
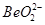 +2H2O
+2H2O(3)Al4C3+4OH-+4H2O===4
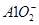 +3CH4↑(方程式2分)
+3CH4↑(方程式2分)(4)将BeCl2加热到熔融状态不能导电证明BeCl2是共价化合物
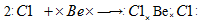 (2分)
(2分)考查元素周期表的结构及常见化学用语的书写。
(1)根据元素周期表的结构可知,Li和Mg位于对角线上,所以二者的性质是相似的。因此Li在空气中燃烧的生成物是Li2O,同时还有Li3N生成。氧化锂是离子化合物,所以电子式是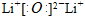 。
。
(2)Be位于第ⅡA族,最高价是+2价,所以最高价氧化物的水化物的化学式是Be(OH)2。既能和酸反应生成盐和水,也能和碱反应生成盐和水的氢氧化物是两性氢氧化物,所以反应的非常适分别是Be(OH)2+2H+===Be2++2H2O、Be(OH)2+2OH-===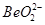 +2H2O。
+2H2O。
(3)由于Be和Al位于对角线关系,所以性质是相似的。则根据反应式Be2C+4H2O===2Be(OH)2+CH4↑可知,Al4C3和水反应应该生成氢氧化铝和甲烷。所以Al4C3遇强碱溶液反应的离子方程式为Al4C3+4OH-+4H2O===4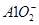 +3CH4↑。
+3CH4↑。
(4)共价化合物在熔融状态下,化学键是不变的,因此共价化合物在熔融状态下不能导电。据此可以鉴别,即将BeCl2加热到熔融状态不能导电证明BeCl2是共价化合物。因此电子式表示BeCl2的形成过程是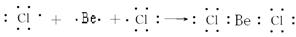 。
。
(1)根据元素周期表的结构可知,Li和Mg位于对角线上,所以二者的性质是相似的。因此Li在空气中燃烧的生成物是Li2O,同时还有Li3N生成。氧化锂是离子化合物,所以电子式是
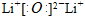 。
。(2)Be位于第ⅡA族,最高价是+2价,所以最高价氧化物的水化物的化学式是Be(OH)2。既能和酸反应生成盐和水,也能和碱反应生成盐和水的氢氧化物是两性氢氧化物,所以反应的非常适分别是Be(OH)2+2H+===Be2++2H2O、Be(OH)2+2OH-===
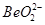 +2H2O。
+2H2O。(3)由于Be和Al位于对角线关系,所以性质是相似的。则根据反应式Be2C+4H2O===2Be(OH)2+CH4↑可知,Al4C3和水反应应该生成氢氧化铝和甲烷。所以Al4C3遇强碱溶液反应的离子方程式为Al4C3+4OH-+4H2O===4
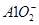 +3CH4↑。
+3CH4↑。(4)共价化合物在熔融状态下,化学键是不变的,因此共价化合物在熔融状态下不能导电。据此可以鉴别,即将BeCl2加热到熔融状态不能导电证明BeCl2是共价化合物。因此电子式表示BeCl2的形成过程是
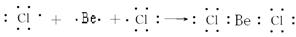 。
。
练习册系列答案
相关题目
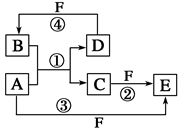

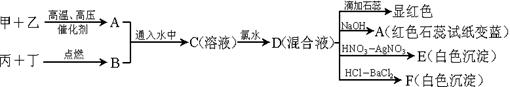

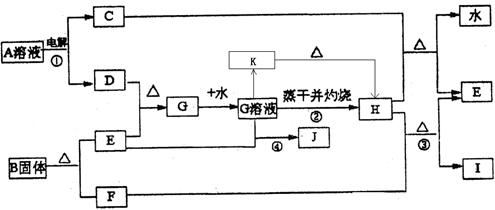
 则样品中G的质量分数为: 。
则样品中G的质量分数为: 。 2CA3(g)
2CA3(g) .0 L.
.0 L.
