题目内容
冶炼金属常用以下几种方法:①以C或CO、H2作还原剂还原;②电解法;③热分解法,现冶炼下列金属Al、Fe、Hg,试标明适宜的冶炼方法(填序号):
Al Fe Hg .
Al
考点:金属冶炼的一般原理
专题:元素及其化合物
分析:Fe、Zn、Cu等中等活泼金属通常用热还原法;
Na、Mg、Al等活泼或较活泼金属通常采用电解法冶炼制备;
Hg、Ag等不活泼金属通常采用热分解法冶炼;
据此分析判断.
Na、Mg、Al等活泼或较活泼金属通常采用电解法冶炼制备;
Hg、Ag等不活泼金属通常采用热分解法冶炼;
据此分析判断.
解答:
解:Na、Mg、Al等活泼或较活泼金属的化合物与C、CO或H2等不反应,故Al采用电解法冶炼制备2Al2O3
4Al+3O2↑,
故答案为:②;
由Fe、Zn、Cu等中等活泼金属用热还原法,即以C、CO或H2做还原剂还原冶炼,铁用热还原法3CO+Fe2O3
2Fe+3CO2;,
故答案为:①;
Hg、Ag等不活泼金属的氧化物不稳定,受热易分解,故汞采用热分解法冶炼,2HgO
2Hg+O2↑,
故答案为:③;
| ||
| 冰晶石 |
故答案为:②;
由Fe、Zn、Cu等中等活泼金属用热还原法,即以C、CO或H2做还原剂还原冶炼,铁用热还原法3CO+Fe2O3
| ||
故答案为:①;
Hg、Ag等不活泼金属的氧化物不稳定,受热易分解,故汞采用热分解法冶炼,2HgO
| ||
故答案为:③;
点评:本题考查了金属的冶炼方法、掌握常见金属的冶炼方法是解题关键,题目较简单.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列物质中既有离子键,又有共价键的是( )
| A、KOH |
| B、CaCl2 |
| C、H2O |
| D、Cl2 |
下列物质中,一定属于同系物的是( )
| A、C2H4 C2H6 |
| B、C2H6 C3H8 |
| C、CH4、C2H4 |
| D、C2H4、C3H4 |
下列判断正确的是( )
| A、Na2S2O3溶液中加入稀硫酸的离子方程式为:2S2O32-+4H+═SO42-+3S↓+2H2O |
| B、用TiCl4制备TiO2的反应可表示为:TiCl4+(x+2)H2O(过量)═TiO2?xH2O↓+4HCl |
| C、滴加甲基橙试液后呈红色的溶液中可以大量共存:Na+、CO32-、K+、AlO2- |
| D、25℃时,pH=12的NaOH溶液中含有OH-的数目为0.01NA |
下列各组物质中,全部属于纯净物的是( )
| A、汽油、油酸、聚乙烯 |
| B、碳酸、盐酸、冰醋酸 |
| C、甘油、乙醇钠、乙酸乙酯 |
| D、福尔马林、食盐、酒精 |
下列电离或水解方程式正确的是( )
| A、Na2SO3的水解:SO32-+2H2O?H2SO3+2OH- |
| B、NaHCO3的电离:NaHCO3?Na++H++CO32- |
| C、KHS溶液中HS-的电离:HS-+H2O?H3O++S2- |
| D、NaClO溶液与FeCl2溶液混合:2ClO-+Fe2++2H2O=2HClO+Fe(OH)2↓ |
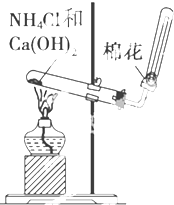 如图是实验室制取的气体发生装置,请结合所学知识,回答下列问题:
如图是实验室制取的气体发生装置,请结合所学知识,回答下列问题: