题目内容
在一定条件下,使10mol SO3在体积固定为2L的密闭容器中发生反应:2SO2(g)+O2(g)?2SO3(g),则下图中正确的是(
表示混合气体的平均相对分子质量)( )
. |
| M |
A、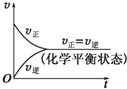 |
B、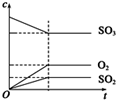 |
C、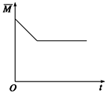 |
D、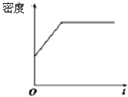 |
考点:化学平衡建立的过程
专题:图示题
分析:A.开始投入SO3,它是生成物,只有逆反应速率,正反应速率为0;
B.据方程式可知SO2比O2生成的多;
C.反应向逆反应进行,据M=
分析;
D.反应向逆反应进行,据ρ=
分析.
B.据方程式可知SO2比O2生成的多;
C.反应向逆反应进行,据M=
| m |
| n |
D.反应向逆反应进行,据ρ=
| m |
| V |
解答:
解:A.开始投入SO3,它是生成物,只有逆反应速率,正反应速率为0,图象上v正、v逆标反了,故A错误;
B.据方程式可知SO2比O2生成的多,下面两条线标的物质反了,故B错误;
C.据M=
,气体的总质量不变,而反应向逆反应方向进行,n变大,故M变小,后来平衡不变了,故C正确;
D.反应向逆反应进行,据ρ=
,气体的总质量不变,体积固定,ρ始终不变,故D错误.
故选C.
B.据方程式可知SO2比O2生成的多,下面两条线标的物质反了,故B错误;
C.据M=
| m |
| n |
D.反应向逆反应进行,据ρ=
| m |
| V |
故选C.
点评:本题考查化学平衡状态的判断与图象的结合,题目难度不大.

练习册系列答案
相关题目
下列说法中正确的是( )
| A、可以利用BaCl2溶液来区分碳酸钾溶液和硫酸钾溶液 |
| B、22.4LO2中一定含有6.02×1023个氧分子 |
| C、在相同温度和压强下,相同体积的任何气体都含有相同数目的粒子 |
| D、0.5 molNaCl溶于0.5L水中得到的溶液的浓度是1.0mol/L |
如图②为恒压容器,①③④为恒容容器,起始加入物如下,且起始容积均相等,维持恒温的条件下发生反应:2SO2(g)+O2(g)?2SO3(g)△H=-197KJ/mol达平衡后,各容器内放出热量Q1、Q2、Q3和Q4的大小关系正确的是( )


| A、197>Q1>Q2 |
| B、Q1>2Q3 |
| C、Q1=Q4 |
| D、Q3<Q4 |
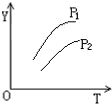 对于密闭容器中的可逆反应:4L(g)?2M(g)+N(g)△H>0,其平衡状态与温度(T)和压强(P1>P2)的关系如图所示.图中y轴是指( )
对于密闭容器中的可逆反应:4L(g)?2M(g)+N(g)△H>0,其平衡状态与温度(T)和压强(P1>P2)的关系如图所示.图中y轴是指( )| A、气体混合物的平均相对分子质量 |
| B、气体混合物的总物质的量浓度 |
| C、L在气体混合物的体积分数 |
| D、气体混合物的密度 |
下列有关电解质溶液中粒子的物质的量浓度关系正确的是( )
| A、在0.1mol?L-1NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) |
| B、在0.1mol?L-1Na2CO3溶液中:c(OH-)-c(H+)═c(HCO4-)+2c(H2CO3) |
| C、向0.2mol?L-1NaHCO3溶液中加入等体积0.1mol?L-1NaOH溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
| D、常温下,pH=7的CH3COONa和CH3COOH混合溶液:c(Na+)+c(CH3COO-)═c(H+)+c(OH-) |
雷雨天闪电时空气中有臭氧(O3)生成.下列说法正确的是( )
| A、O2和O3互为同位素 |
| B、O2和O3的相互转化是物理变化 |
| C、在相同的温度与压强下,等体积的O2和O3含有相同的分子数 |
| D、等物质的量的O2和O3含有相同的质量 |
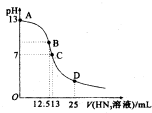 氮气是空气中含量最多的一种气体,氮气及其化合物在工农业生产、生活中有着广泛的应用.请回答下列问题:
氮气是空气中含量最多的一种气体,氮气及其化合物在工农业生产、生活中有着广泛的应用.请回答下列问题: