题目内容
6.下列有关化学反应能量变化的叙述中,正确的是( )| A. | 只要是在加热条件下进行的反应一定是吸热反应 | |
| B. | 一种能量形式可以转化为另外的能量,所以任何反应都可以把化学能转化为电能 | |
| C. | 中和反应和燃烧是放热反应,Ba(OH)2•8H2O与NH4Cl的反应是吸热反应 | |
| D. | 只要反应物的总能量高于生成物的总能量,在任何条件下该反应就能够发生 |
分析 A、需要加热才能进行的反应不一定是吸热反应;
B、只有氧化还原反应才能将化学能转变为电能;
C、酸碱中和反应和燃烧反应均为放热反应,Ba(OH)2•8H2O与NH4Cl的反应是吸热反应;
D、只要反应物的总能量高于生成物的总能量,只能说明该反应为放热反应.
解答 解:A、需要加热才能进行的反应不一定是吸热反应,如木炭的燃烧是放热的,但也需要加热才能发生,故A错误;
B、只有氧化还原反应才能将化学能转变为电能,没有电子的得失或偏移的反应不能将化学能转变为电能,故B错误;
C、酸碱中和反应和燃烧反应均为放热反应,Ba(OH)2•8H2O与NH4Cl的反应是典型的吸热反应,故C正确;
D、只要反应物的总能量高于生成物的总能量,只能说明该反应为放热反应,但该反应不一定在任何条件下均能发生,故D错误.
故选C.
点评 本题考查了常见的吸放热反应和反应发生的条件以及能量的转化形式,应注意的是能将化学能转变为电能的只有氧化还原反应.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.表是元素周期表的一部分,请回答有关问题:
(1)表中化学性质最不活泼的元素其原子结构示意图为 .
.
(2)表中能形成两性氢氧化物的元素其单质与⑨最高价氧化物的水化物反应的化学方程式2Al+2KOH+2H2O=2KAlO2+3H2↑.
(3)④元素与⑦元素形成化合物的电子式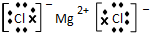 .
.
(4)①、②、⑥、⑦四种元素的最高价氧化物的水化物中酸性最强的是HClO4(填化学式).
(5)在⑨与④的单质中,化学性质较活泼的是K,①、②的气态氢化物中,比较稳定的是NH3(填化学式).
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
 .
.(2)表中能形成两性氢氧化物的元素其单质与⑨最高价氧化物的水化物反应的化学方程式2Al+2KOH+2H2O=2KAlO2+3H2↑.
(3)④元素与⑦元素形成化合物的电子式
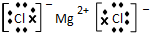 .
.(4)①、②、⑥、⑦四种元素的最高价氧化物的水化物中酸性最强的是HClO4(填化学式).
(5)在⑨与④的单质中,化学性质较活泼的是K,①、②的气态氢化物中,比较稳定的是NH3(填化学式).
17.检验某未知溶液中是否含SO42-的下列操作中,合理的是( )
| A. | 先加硝酸酸化,再加氯化钡溶液 | B. | 先加硝酸酸化,再加硝酸钡溶液 | ||
| C. | 先加盐酸酸化,再加氯化钡溶液 | D. | 先加盐酸酸化,再加硝酸铜溶液 |
14.化学与社会、生产、生活密切相关.下列说法不正确的是( )
| A. | 硅胶可用作食品干燥剂 | B. | 乙醇可作消毒剂 | ||
| C. | 氢氧化铝可作胃酸中和剂 | D. | 二氧化碳可作钠着火的灭火剂 |
1.下列物质中,既含有离子键,又含有非极性共价键的是( )
| A. | Na2O2 | B. | CaCl2 | C. | NaOH | D. | NH4Cl |
18.在生活、生产及化学研究中,人们经常需要根据不同原子、分子或离子的某些特征反应对物质进行检验,以确定物质的组成.下列有关物质检验的说法正确的是( )
| A. | MnO2、CuO、Fe三种物质的粉末都是黑色的,用稀盐酸不能将它们区别开 | |
| B. | (NH4)2SO4、K2SO4、NH4C1三种物质不能用一种试剂通过化学反应区别开 | |
| C. | 可以用BaCl2溶液和稀硝酸检验Na2SO3 是否变质 | |
| D. | 用湿润的KI淀粉试纸可以检验氯化氢气体中是否含有氯气 |
15.下列说法不正确的是( )
| A. | 质子数相同的粒子一定属于同一种元素 | |
| B. | 同一元素的核素种数由中子数决定 | |
| C. | 同位素的化学性质几乎相同 | |
| D. | 质子数相同、电子数也相同的两种粒子,不可能是一种分子和一种离子 |
16.可用如图装置制取(必要时可加热)、净化、收集的气体是( )
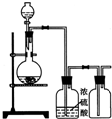

| A. | 铜和稀硝酸制一氧化氮 | B. | 亚硫酸钠与浓硫酸制二氧化硫 | ||
| C. | 锌和稀硫酸制氢气 | D. | 烧碱固体与浓氨水制氨气 |
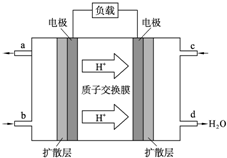 人们应用原电池原理制作了多种电池以满足不同的需要.电池发挥着越来越重要的作用,如在宇宙飞船、人造卫星、电脑、照相机等,都离不开各式各样的电池,同时废弃的电池随便丢弃也会对环境造成污染.请根据题中提供的信息,回答下列问题:
人们应用原电池原理制作了多种电池以满足不同的需要.电池发挥着越来越重要的作用,如在宇宙飞船、人造卫星、电脑、照相机等,都离不开各式各样的电池,同时废弃的电池随便丢弃也会对环境造成污染.请根据题中提供的信息,回答下列问题: