题目内容
下列各组中的离子,能在溶液中大量共存的是( )
| A、H+、Na+、CO32- |
| B、Ba2+、Na+、SO42- |
| C、K+、H+、OH- |
| D、Ag+、NO3-、H+ |
考点:离子共存问题
专题:离子反应专题
分析:A.氢离子与碳酸根离子发生反应,在溶液中不能共存;
B.钡离子与硫酸根离子反应生成硫酸钡沉淀;
C.氢离子与氢氧根离子反应生成水,在溶液中不能大量共存;
D.Ag+、NO3-、H+离子之间不反应,在溶液中能够大量共存.
B.钡离子与硫酸根离子反应生成硫酸钡沉淀;
C.氢离子与氢氧根离子反应生成水,在溶液中不能大量共存;
D.Ag+、NO3-、H+离子之间不反应,在溶液中能够大量共存.
解答:
解:A.H+、CO32-之间能够发生反应,在溶液中不能大量共存,故A错误;
B.Ba2+、SO42-之间能够发生反应生成难溶物硫酸钡,在溶液中不能大量共存,故B错误;
C.H+、OH-离子之间反应生成水,在溶液中不能大量共存,故C错误;
D.Ag+、NO3-、H+之间不满足离子反应发生条件,在溶液中可以大量共存,故D正确;
故选D.
B.Ba2+、SO42-之间能够发生反应生成难溶物硫酸钡,在溶液中不能大量共存,故B错误;
C.H+、OH-离子之间反应生成水,在溶液中不能大量共存,故C错误;
D.Ag+、NO3-、H+之间不满足离子反应发生条件,在溶液中可以大量共存,故D正确;
故选D.
点评:本题考查离子共存的正误判断,该题是高考中的高频题,属于中等难度的试题,侧重对学生基础知识的训练和检验,注意明确离子不能大量共存的一般情况,如:(1)能发生复分解反应的离子之间;(2)能生成难溶物的离子之间;(3)能发生氧化还原反应的离子之间;(4)能发生络合反应的离子之间(如 Fe3+和 SCN-).

练习册系列答案
相关题目
下列离子方程式书写正确的是( )
| A、向氧化铁中加入氢碘酸:Fe2O3+6H++2I-=2Fe2++I2+3H2O | ||||
| B、Cu片插入FeCl3溶液中:Cu+Fe3+═Fe2++Cu2+ | ||||
C、向Al2(SO4)3溶液中加入过量的氨水:Al3+4NH3?H2O═Al
| ||||
D、向NaHSO4溶液中滴加Ba(OH)2溶液至中性:H++S
|
下列各组离子能够大量共存的是( )
| A、pH=0的溶液中:Fe3+、Mg2+、Cl-、SO42- |
| B、使pH试纸显蓝色的溶液中:Cu2+、Fe3+、NO3-、SO42- |
| C、滴入甲基橙指示剂呈红色的溶液中:Na+、NH4+、CO32-、NO3- |
| D、水电离出的c(H+)=1×10-13mol?L-1的溶液中:K+、HCO3-、Cl-、NH4+ |
如图是一套电化学装置,对其有关说法错误的是( )

| A、装置A是原电池,装置B是电解池 |
| B、反应一段时间后,装置B中溶液PH增大 |
| C、a口若消耗1mol CH4,d口可产生4mol气体 |
| D、a口通入C2H6时的电极反应为 C2H6-14e-+18OH-═2CO32-+12H2O |
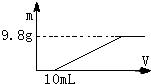 过量的硝酸和6.4g铜充分反应,向反应后的溶液中滴加5mol?L-1的氢氧化钠溶液,加入氢氧化钠溶液的体积与生成沉淀的关系如图所示,则反应后溶液中所含NO3-的物质的量为( )
过量的硝酸和6.4g铜充分反应,向反应后的溶液中滴加5mol?L-1的氢氧化钠溶液,加入氢氧化钠溶液的体积与生成沉淀的关系如图所示,则反应后溶液中所含NO3-的物质的量为( )| A、0.05mol |
| B、0.1mol |
| C、0.2mol |
| D、0.25mol |
下列离子方程式书写错误的是( )
| A、向KHSO4溶液中滴入Ba(OH)2溶液使pH=7:SO42-+H++Ba2++OH-=BaSO4↓+H2O |
| B、少量小苏打溶液滴入Ba(OH)2溶液中:HCO3-+Ba2++OH-=BaCO3↓+H2O |
| C、碳酸氢根离子发生电离:HCO3-+H2O?H3O++CO32- |
| D、将1mol?L-1 NaAlO2溶液和1.5mol?L-1 HCl溶液等体积互相均匀混合:6AlO2-+9H++3H2O=5Al(OH)3↓+Al3+ |