题目内容
在给定条件下,下列划线的物质在化学反应中能被完全消耗的是( )A.在适当温度和催化剂作用下,用2molSO2和1molO2合成SO3
B.标准状况下,将1g铝片投入20mL18mol?L-1的硫酸中
C.常温下,向100mL3mol?L-1的硝酸中加入6.4gCu
D.将含有少量H2O(g)的H2通入足量Na2O2容器中并不断用电火花点燃
【答案】分析:A、可逆反应不能完全反应.
B、Al与浓硫酸在常温下发生钝化现象.
C、铜与稀硝酸反应,根据过量计算判断铜与硝酸的剩余情况.
D、由于电火花的引燃,氢气与生成的氧气反应生成水,水再与过氧化钠反应生成氧气,如此循环反应,相当于H2与Na2O2反应生成NaOH.
解答:解:A、二氧化硫和氧气反应生成三氧化硫的反应是可逆反应,存在反应限度,不能完全反应,故A错误.
B、18mol/L的浓硫酸在标况下能与Al发生钝化,生成的致密氧化物薄膜阻止反应的进一下发生,则Al不会被完全反应掉,故B错误.
C、n(Cu)=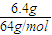 =0.1mol,n(HNO3)=0.1mL×3mol?L-1=0.3mol,根据方程式3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O可知,0.1molCu完全反应需硝酸0.8mol,所以Cu有剩余,故C错误.
=0.1mol,n(HNO3)=0.1mL×3mol?L-1=0.3mol,根据方程式3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O可知,0.1molCu完全反应需硝酸0.8mol,所以Cu有剩余,故C错误.
D、由于电火花的引燃,氢气与生成的氧气反应生成水,水再与过氧化钠反应生成氧气,如此循环反应,相当于H2与Na2O2反应生成NaOH,过氧化钠足量,所以氢气完全反应,故D正确.
故选:D.
点评:本题考查物质的性质、过量计算、可逆反应等,学会过量计算.易错选项是B,注意铁、铝和浓硫酸、浓硝酸发生钝化现象,D项是学生解答的难点,利用循环反应,弄清构成循环的因素,找出完全反应时的总反应方程式,再依据一般的过量计算即可使问题迎刃而解.
B、Al与浓硫酸在常温下发生钝化现象.
C、铜与稀硝酸反应,根据过量计算判断铜与硝酸的剩余情况.
D、由于电火花的引燃,氢气与生成的氧气反应生成水,水再与过氧化钠反应生成氧气,如此循环反应,相当于H2与Na2O2反应生成NaOH.
解答:解:A、二氧化硫和氧气反应生成三氧化硫的反应是可逆反应,存在反应限度,不能完全反应,故A错误.
B、18mol/L的浓硫酸在标况下能与Al发生钝化,生成的致密氧化物薄膜阻止反应的进一下发生,则Al不会被完全反应掉,故B错误.
C、n(Cu)=
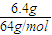 =0.1mol,n(HNO3)=0.1mL×3mol?L-1=0.3mol,根据方程式3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O可知,0.1molCu完全反应需硝酸0.8mol,所以Cu有剩余,故C错误.
=0.1mol,n(HNO3)=0.1mL×3mol?L-1=0.3mol,根据方程式3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O可知,0.1molCu完全反应需硝酸0.8mol,所以Cu有剩余,故C错误. D、由于电火花的引燃,氢气与生成的氧气反应生成水,水再与过氧化钠反应生成氧气,如此循环反应,相当于H2与Na2O2反应生成NaOH,过氧化钠足量,所以氢气完全反应,故D正确.
故选:D.
点评:本题考查物质的性质、过量计算、可逆反应等,学会过量计算.易错选项是B,注意铁、铝和浓硫酸、浓硝酸发生钝化现象,D项是学生解答的难点,利用循环反应,弄清构成循环的因素,找出完全反应时的总反应方程式,再依据一般的过量计算即可使问题迎刃而解.

练习册系列答案
相关题目
|
在给定条件下,下列划横线的物质在对应的化学反应中能完全耗尽的是 | |
| [ ] | |
A. |
标准状况下,将1 g铝片投入20 mL 18.4 mol/L的硫酸中 |
B. |
向100 mL 5 mol/L的硝酸中加入5.6 g铁 |
C. |
用40 mL 10 mol/L的盐酸与10 g二氧化锰共热制取氯气 |
D. |
在高温高压和有催化剂的条件下,用1.2 mol氮气和3 mol氢气合成氨 |
在给定条件下,下列划横线的物质在对应的化学反应中能完全耗尽的是
| A.标准状况下,将1 g铝片投入20 mL 18.4 mol/L的硫酸中 |
| B.向100 mL 5 mol/L的硝酸中加入5.6 g铁 |
| C.用40 mL 10 mol/L的盐酸与10 g二氧化锰共热制取氯气 |
| D.在高温高压和有催化剂的条件下,用1.2 mol氮气和3 mol氢气合成氨 |