题目内容
下列热化学方程式中,△H能正确表示物质的燃烧热的是( )
| A、S(s)+O2(g)=SO2(g)△H=-269.8 kJ/mol | ||
B、C(s)+
| ||
C、H2(g)+
| ||
| D、2C8H18+(l)25O2(g)=16CO2(g)+18 H2O(l)△H=-11036 kJ/mol |
考点:燃烧热
专题:化学反应中的能量变化
分析:燃烧热表示1mol可燃物完全燃烧生成稳定氧化物所放出的热量,表示燃烧热的热化学方程式中可燃物为1mol,产物为稳定氧化物.
解答:
解:A、S的化学计量数为1,产物为稳定氧化物,△H代表燃烧热,故A正确;
B、C的化学计量数为1,但产物不是稳定氧化物,碳的稳定氧化物为二氧化碳,所以△H不代表燃烧热,故B错误;
C、H2的化学计量数为1,但产物不是稳定氧化物,所以△H不代表燃烧热,故C错误;
D、C8H18的化学计量数为2,产物是稳定氧化物,△H不代表燃烧热,故D错误;
故选:A.
B、C的化学计量数为1,但产物不是稳定氧化物,碳的稳定氧化物为二氧化碳,所以△H不代表燃烧热,故B错误;
C、H2的化学计量数为1,但产物不是稳定氧化物,所以△H不代表燃烧热,故C错误;
D、C8H18的化学计量数为2,产物是稳定氧化物,△H不代表燃烧热,故D错误;
故选:A.
点评:本题考查了燃烧热的概念,表示燃烧热的热化学方程式中可燃物为1mol,产物为稳定氧化物,碳形成二氧化碳、氢形成液态水,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
设NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A、1mol甲醇中含有C-H键的数目为4NA |
| B、Na2O2与足量H2O反应产生0.2mol O2,转移电子的数目为0.4NA |
| C、25℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA |
| D、标准状况下,2.24L己烷含有分子的数目为0.1NA |
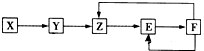 五种常见物质X、Y、Z、E、F均含有同一元素M,已知Y是单质,Z是NO(一氧化氮),在一定条件下它们有如图转化关系,下列推断不合理的是( )
五种常见物质X、Y、Z、E、F均含有同一元素M,已知Y是单质,Z是NO(一氧化氮),在一定条件下它们有如图转化关系,下列推断不合理的是( )| A、M元素可能是非金属元素,也可能是金属元素 |
| B、X可能是一种氢化物 |
| C、E可能是一种有色气体 |
| D、X→Y可能是非氧化还原反应 |
CO2与H2的混合气体4.6g和足量的氧气混合,在120℃时用电火花充分引燃,相同状况下将反应所得混合气体通入足量的Na2O3中,测得Na2O3固体质量增重3g,则原混合气体中CO2的物质的量分数为( )
| A、25% | B、50% |
| C、75% | D、96% |
根据中学化学课本中的数据资料作出以下推断,其中不正确的是( )
| A、利用密度数据可判断液体物质挥发性的大小 |
| B、利用化合价数据可以确定某些元素原子的最外层电子数 |
| C、利用原子半径数据可推断某些原子的氧化性和还原性的强弱 |
| D、利用溶解度数据可推测将一些物质混合物分离开来的可能性 |
已知KCl在某温度时的溶解度为29.8g.在此温度下KCl饱和溶液的密度为1.15g/cm3,则100mL该饱和溶液中KCl的物质的量浓度约为( )
| A、0.4mol/L |
| B、4.0mol/L |
| C、0.35mol/L |
| D、3.5mol/L |
下列各组物质的稀溶液相互反应,无论是前者滴入后者,还是后者滴入前者,反应现象都相同的是( )
| A、Na2CO3和HCl |
| B、NaHCO3和Ba(OH)2 |
| C、NaAlO2和H2SO4 |
| D、AgNO3和NH3?H2O |